Az aminosavak biológiai szerepe és alkalmazása
Mi az aminosavak biológiai szerepe? Próbáljunk együtt találni a választ erre a kérdésre. Megmutatjuk ennek a szervesanyag-csoportnak a sajátosságait, azok kémiai tulajdonságait, a fő alkalmazási területeket.
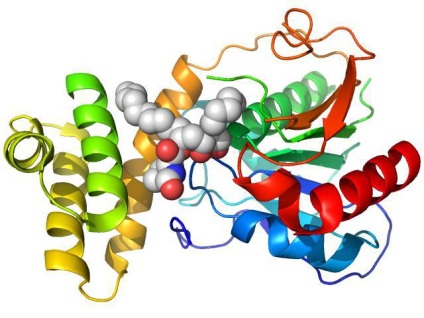
Történelmi háttér
Az első nyílt aminosav a glicin volt. 1820-ban szintetizálták a zselatin savas hidrolízisével. A proteinmolekulák aminosav-összetételének megfejtése csak a múlt század közepén volt lehetséges, majd kiderült az aminosav - treonin.
Főbb funkciók
Jelenleg 300 aminosavról van információ, amelyek különböző funkciókat töltenek be a szervezetben.
Mi az aminosavak fő biológiai szerepe? Huszonegyet standardnak (fehérjéknek) tekintünk, mivel ezek a fő fehérjemolekulák részét képezik.
Ezek a vegyületek bizonyos fehérjék részét képezik. Az oxiprilin az alapja a kollagénnek, az elasztint dezmosin alkotja.
Közbenső anyagok lehetnek az anyagcsere folyamatokban. Ezt a funkciót citrullin, ornitin végzi.
Az aminosavak biológiai funkciója magában foglalja a nukleotidok, poliamidok szintézisét is. E vegyületek szénláncát más szerves anyagok előállítására használják:
- glükóz glükogén aminosavakból szintetizálódik;
- a lipideket ketogén vegyületek alkotják.
Az aminosavak biológiai szerepe a funkcionális csoportok meghatározásában rejlik. A ciszteint akkor használják, amikor szulfátcsoportot észlelnek. Az aszpartátot egy aminocsoport kimutatásában használják.

Nómenklatúra jellemzői
Milyen helyesen nevezik az aminosavakat? E vegyületek szerkezetét, osztályozását és biológiai szerepét az iskola tanterve is figyelembe veszi.
Az aminosavak karbonsavak származékai, amelyekben egy hidrogénatomot aminocsoporttal helyettesítünk.
E funkcionális csoport helyétől függően az egyik vegyület több izomert tartalmazhat. A vegyészek egyszerre három különböző nómenklatúrát használnak: racionális, triviális, szisztematikus.
Ezeknek a vegyületeknek a triviális neve az elkülönített forráshoz kapcsolódik. A szerin szerepel a fibroin selymben, a glutamin megtalálható a gabona növények gluténében. Cisztin jelen van a hólyag köveiben.
A racionális név a karbonsavszármazékhoz kapcsolódik, és a rövidített megnevezés a fehérjemolekula aminosavainak szekvenciáját jelöli. A biokémiában e vegyületek rövidített és triviális nevét használják.
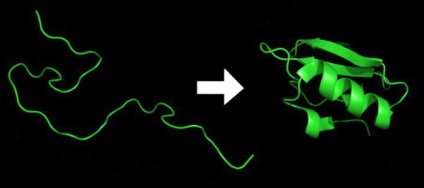
Az aminosavak osztályozása
Annak érdekében, hogy megértsük az aminosavak biológiai szerepét és azok felhasználását, inkább részletesebben megoszthassuk ezeket a szerves vegyületek besorolásának típusát.
Jelenleg többféle besorolást használnak:
- radikálisan;
- polaritásának mértékével;
- a test szintézisének variánsairól.
A szerves kémiai szerkezetben a különböző aminosavak izoláltak.
Az alifás vegyületek egy karboxilcsoportot és egy aminocsoportot tartalmazhatnak, mely esetben monoamino-karbon-vegyületek.
Két COOH és egy aminocsoport jelenlétében az anyagokat monoamino-dikarbonsavaknak nevezik.
Emellett az aminosavak diaminomonokarbonsav- és diamino-dikarbonsavjait is izoláljuk.
A ciklikus fajok nemcsak a ciklusok számában különböznek, hanem a minőségi összetételükben is.
Lenin szerint az aminosavak négy csoportra vannak osztva a szénhidrogén-radikális vízzel való kölcsönhatásának jellemzői szerint:
- hidrofób;
- hidrofil;
- negatívan felszámolt;
- pozitív töltésű.
Attól függően, hogy az aminosavak mennyire képesek szintetizálni az emberi testben, elengedhetetlenek (táplálékkal), valamint cserélhető fajok.
Számos tudományos kísérlet bizonyította az alfa-aminosavak biológiai szerepét.
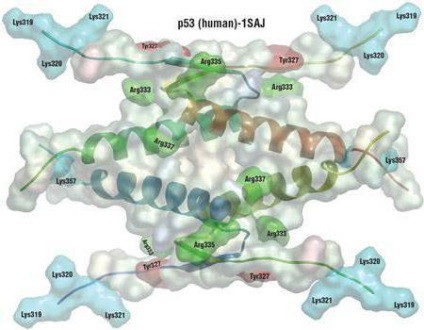
Fizikai tulajdonságok
Milyen tulajdonságokkal rendelkeznek az aminosavak? A vegyületek nómenklatúráját, tulajdonságait és biológiai szerepét az egyetemes kémiai állapotvizsgálat során az iskolák végzős hallgatóinak kínálják. Ezek a szerves savak nagyon jól oldódnak vízben, magas olvadásponttal rendelkeznek.
Optikai aktivitását az aszimmetrikus szénatom molekuláin való jelenlét magyarázza (kivéve a glicint önmagában). Ezért találták meg az aminosavak L- és D-sztereoizomerjeit.
Az L-sorozatú izomereket állati fehérjékben találjuk. A hidrogénindex értéke ezen vegyületek esetében az 5,5-7 tartományba esik.
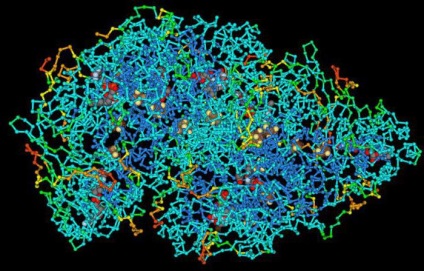
Kémiai tulajdonságok
Tekintsük az aminosavakat részletesebben. Ezeknek a szerves anyagoknak a szerkezetét, kémiai tulajdonságait, biológiai szerepét ismerni kell.
Az aminosavak kémiai tulajdonságainak specifitása kettősségükben rejlik. Az amfoteritás oka két funkciós csoport jelenléte ezen szerves savakban.
A COOH karboxilcsoport jelenléte ezeknek a vegyületeknek savas jellegű. Gyakran kölcsönhatásba léphetnek az aktív fémekkel, bázikus oxidokkal, lúgokkal. Ezen szerves vegyületek tulajdonságainak savasságát az észterezési reakcióban (éterekkel, észterekkel) is meg lehet mutatni.
Az aminosavak kémiai kölcsönhatásba léphetnek a gyenge ásványi savakkal alkotott sókkal is. Az ilyen reakció példájaként az aminosavak bikarbonátokkal és karbonátokkal való kölcsönhatását vizsgálhatjuk.
Ennek az osztálynak fő tulajdonságai az aminosavaknak az aminocsoport egyéb savakkal való reakciója. Ebben az esetben sók képződnek.
Az aminosavak dekarboxilezésének biológiai szerepe az, hogy egy semleges tápközeg keletkezik, ami teljesen biztonságos az élő szervezet számára.
A ninhidrin reakció lehetővé teszi az aminosavak kimutatását egy oldatban. A reakció lényege, hogy egy aminosavval kölcsönhatásba lépő ninhidrin színtelen oldata dimer formában kondenzálódik egy nitrogénatomon keresztül, amely a megfelelő sav aminocsoportjából leválik.
Az eredményül kapott pigment vörös-filiiitin színárnyalatú, továbbá az aminosav dekarboxilezése bizonyos aldehid és szén-monoxid képződését eredményezi (4).
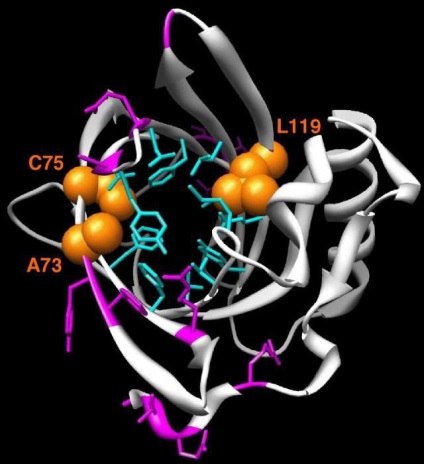
Specifikus reakciók
Az aminosavakban a karboxil- és aminocsoportokon kívül további funkcionális csoportok is jelen lehetnek. A kutatólaboratóriumokban való elkötelezettségük minőségi reakciókat folytat.
Az arginin kimutatható a minőségi Sakaguchi reakcióban (a guanidin csoporton). A ciszteint az SH csoporthoz specifikus Fole módszerrel határozhatjuk meg.
A nitrálási reakció (xantoprotein reakció) lehetővé teszi az aromás aminosav jelenlétét a keverékben. A Millon reakciót úgy alakították ki, hogy azonosítsa a hidroxilcsoportot a tirozin aromás gyűrűjében.
A peptidkötés jellemzői
Milyen tulajdonságokkal rendelkeznek a kéntartalmú aminosavak? Biológiai szerepe a peptidmolekulák kialakulásához kapcsolódik. Ha több aminosavmolekula kölcsönhatásba lép egymással, a vízmolekulák hasadódnak, és az aminosavmaradékok peptiid (amid) kötéseket alkalmazva peptideket képeznek.
A polipeptidet alkotó aminosavmaradékok száma jelentősen változik. Azokat a peptideket, amelyek nem tartalmaznak tíz aminosav-maradékot, oligopeptideknek nevezik. A kapott vegyület nevét gyakran az aminosavmaradékok száma jelzi.
Ha az anyag több mint tíz aminosavat tartalmaz, akkor a vegyületeket polipeptideknek nevezik. Azoknál a vegyületeknél, amelyek több mint ötven aminosavmaradékot tartalmaznak, szintézisük terméke fehérje.
Tehát a glukagon hormon, amely 29 aminosavat tartalmaz, hormonnak nevezzük. Az aminosavmaradékok a kiindulási szerves savak monomerek, amelyekből a fehérje-vegyületek képződnek.
A bal oldalon írt aminosav aminosavcsoportot N-terminálisnak nevezünk, egy karboxilcsoportot tartalmazó fragmenst C-terminálisnak tekintünk, szokásos a jobb oldalon írni.
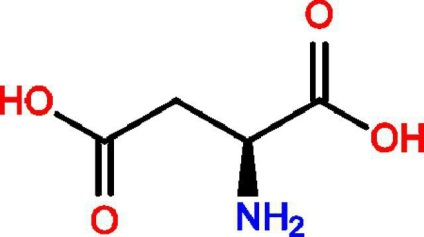
Néhány aminosav fontossága
A glicin (aminoecetsav) a szén-fragmensek adományozója, amelyek a hemoglobin, a pirrol, a kolin, a nukleotidok, valamint a kreatin szintéziséhez szükségesek.
A szerin jelen van az aktív enzimközpontokban. Ez az aminosav szükséges a foszfoprotein (természetes tej kazein) szintéziséhez.
Glucogénsav szükséges a fehérje molekula másodlagos, tercier struktúrájának kialakításához. Ebben a vegyületben a leginkább reaktív aktív funkciós csoport van, ezért az anyag könnyen belép a redox folyamatokba, megköti a nehézfémeket oldhatatlan vegyületek formájában. A kéntartalmú anyagok szintéziséhez szükséges szulfátcsoport adományozójának feladata.
következtetés
Az aminosavak amfoter szerves vegyületek, amelyeknek fontos biológiai jelentősége van. A szintézisben lévő aminosavmaradékok a fehérje molekula elsődleges szerkezetét képező szekvenciát alkotnak. Attól függően, hogy pontosan az aminosav-fragmensek épülnek-e, az egyes élő szervezetekre specifikus fehérje szintetizálódik.

Listája legdrágább amerikai kúriák hazafelé a 250 millió $ a közelmúltban épült Bel Air kúriát eladásra a 250 millió $, ami a legdrágább házat eladta a pillanatban az Egyesült Államokban.

10 őrült egybeesés, amit nehéz elhinni Minden egyes ember életében volt némi véletlen. Előfordul, hogy olyan barátra gondolsz, akit sok év óta nem láttak, majd hirtelen be van építve.
