A helyi érzéstelenítés élettani és farmakológiai jellemzői
A helyi érzéstelenítés élettani és farmakológiai jellemzői
Az összes helyi érzéstelenítő molekulája három fő összetevőből áll: a lipofil részből, a hidrofil aminból és a középső láncból. A lipofil része lehetővé teszi, hogy a helyi érzéstelenítő behatolnak szubsztrátok zsírsejtek idegszövetben, gidrofilicheskaya (amin) egy részét nyújtja a bomlási a molekula és annak behatolását az intersticiális folyadék az ideg.
A nagyon hatékony anesztetikumok kiegyensúlyozott tulajdonságokkal rendelkeznek. Különösen, ha az ágensnek nincs megfelelően kimutatott hidrofil része, vagy megfosztották, akkor csak alkalmazásokhoz alkalmazható, azaz. felületesen. Az érzéstelenítés hatékonysága számos tényezőtől függ, amelyek közül a legfontosabb a szövetek CBS-je. Normális esetben a szövetfolyadék pH-ja 7,3-7,4; Az érzéstelenítő oldat pH-ja 3,8-6,5 között változik. A savas oldali pH-eltolódás esetén az érzéstelenítők nagy része kationokkal van kitéve, ami biztosítja annak hatékonyságát. Ha a gyulladás a szöveti pH csökken, hogy 6,0 vagy ennél kisebb, és ezáltal csökkentve a érzéstelenítő belépő az ideg és a kationok feleslegben, ez nem mutat a szükséges aktivitással. Tehát bármely érzéstelenítő hatásossága a szövet pH-értékétől függ.
Neurofiziológia. A helyi érzéstelenítés központi eleme az impulzus átvitelének érzékenyen történő leállítása
idegrostok és a receptorok blokkolása. Az idegmembránon ható érzéstelenítés megakadályozza annak depolarizációját, amely nélkül nem lehet idegimpulzus végrehajtani. Az idegsejtek közvetlenül vagy közvetve részt vesznek az idegmembrán metabolizmusának és táplálkozásának folyamatában, amely felelős a pulzus generálásáért és továbbításáért. A membrán lökést ad a perifériától a középpontig. Ha a pulzusszaporítás megszakad, akkor a fájdalom megszűnik. A membrán egy bimolekuláris lipidréteg, amely polipeptidek monomolekuláris rétegei között helyezkedik el. Amint az 1. ábrán látható. 1, fehérje-, zsír- és fehérjehéjakból áll, amelyeket jen, axoplazma és extracelluláris folyadék választ el.
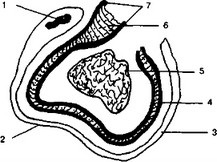
Ábra. 1 ideg 1 szakasza - mag, Schwann 2 sejtje, 3 - mielin; 4 - idegmembrán; 5 - axoplasma; 6 - lipidréteg, 7 - fehérjehéj.
Az idegmembrán metabolizmusával monitorozzák a különböző ionok koncentrációját az intersticiális folyadékban. Az ioncsíkok változása a depolarizációhoz és az impulzus terjedésének irányához vezet. Nagy kóros körülményekkel szembeni külső ellenállóképessége kálium-, nátrium-, kloridionok áthaladásának megsértésével jár, amelyek általában rendesen behatolnak akadálytalanul.
A mielin idegrostok réteg veszi körül, amely található az ideg a henger alakú álló lemmotsitov (Schwann-sejtek), és megvédi azt a külső behatásoktól. A myelin abszorpciós gát, és a helyi érzéstelenítők nem tudnak mindig behatolni. A mielinázott réteg megszakítható, az idegmembránt ki lehet téve. Ezek az áttörések csomóként ismertek. Ezekben a helyeken az érzéstelenítő megoldások könnyen diffundálnak az idegmembránba, ami idegi gátlást okoz.
A lendület terjedése. A keletkező elektromos impulzus egy gyorsan változó membránpotenciál, amely a fájdalomponttól egy depolarizációs hullám útján terjed, akciópotenciálnak nevezzük. Pihenőállapotban a membrán külső felülete pozitív töltésű, a belső felülete negatív. Amikor egy inger jelenik meg, lassan egy bizonyos szintre emelkedik, amit az idegrost küszöbének neveznek. Amikor ez a küszöb eléri a kritikus szintet, a depolarizáció bekövetkezik. Ha a kritikus szintet nem éri el, akkor az impulzus nem merül fel (az "egész vagy semmi" elve). A küszöbérték elérése után a potenciális különbség megnő, majd repolarizáció következik be, és a membránpotenciál visszatér a kezdeti szintre, amit nyugalmi állapotban figyeltek meg. A depolarizáció és a repolarizáció az idegrost teljes hosszában megy végbe. A pihentető idegmembrán a nátriumionok gátja. A depolarizáció során a nátriumion a membránon keresztül mozog a nátriumcsatornán. A potenciál megváltoztatása káliumionok felszabadulását eredményezi ("nátrium-szivattyú"). Ez új akciós potenciálot és a potenciálkülönbség csökkenését eredményezi az egész membránon.
A fentiek mindegyike összefoglalva fejezhető ki: a modern fogalmak szerint a gerjesztés és a membrán permeabilitásának átviteli folyamata a sejt állapotától függ. A pulzusszaporítás három szakaszból áll: polarizáció, depolarizáció és repolarizáció. Az első szakaszban a kálium intracelluláris koncentrációja meghaladja a nátrium koncentrációját, ami megakadályozza
negatív potenciál (pihenő potenciál) megjelenése a membrán belső felületén, intracelluláris anionokkal. A nátriumionok helyzete szintén stabil, mivel nem tud belépni a sejtbe, mert a polarizáció miatt a membrán jelenleg alacsonyan áteresztő a nátrium számára (2. Később, amikor a nyugalmi potenciál a megfelelő küszöbértékhez képest csökken, a membrán permeabilitása nő a nátriumionok számára, amelyek ionos és elektrosztatikus gradiensek hatására átjutnak a sejtbe. Ennek eredményeképpen a membrán depolarizációja bekövetkezik, és pozitív hatásmutató jelenik meg, amely elősegíti az idegsejt mentén fellépő impulzust (3. A gerjesztést követõen egy refrakter periódus jelentkezik, amelyben a membrán potenciálja csökken a nyugalmi potenciál értékéhez képest. A repolarizáció állapotában az idegsejt felkészül a más impulzus észlelésére és végrehajtására (Shchekunov, B.C., 1976).
A helyi érzéstelenítők hatásmechanizmusa az impulzusok terjedésének gátlása, és a membrán permeabilitásának megváltoztatása a nátriumionok számára, így depolarizációja lehetetlen. Hasonlóképpen, a káliumionok membrán permeabilitása is változik, de kisebb mértékben. A helyi érzéstelenítés hatására,
2. ábra Idegi membrán nyugalmi állapotban
- - extracelluláris
folyékony;
- - nátriumcsatorna.
- - káliumcsatorna,
- - axoplazma
na cos, és így a küszöbértéket elérjük. Lényegében a depolarizáció jelensége összefügg a nátriumionok nátriumcsatornákon történő előrehaladásával. Úgy gondolják, hogy az összes helyi érzéstelenítő hatását az idegmembrán nátriumcsatornáinak átjárhatósága megváltoztatja. Lidocaine, prokain, mepivokain kötődnek a receptorokhoz, található, a külső felületén az idegi membrán nátrium-csatornák (ábra. 4) (Allen G. D. 1984).
Az akciós potenciál előfordulása gerjesztés terjedését eredményezi az idegrost más részeiben, a nátriumionok penetrációjába az axoplazmába és a káliumionok felszabadulásához ("nátrium-kálium-szivattyú"). Ezt a folyamatot kalciumionok szabályozzák, amikor ezeknek a sejteknek a koncentrációja nő az extracelluláris folyadékban, a membrán küszöb nő. Ismert, hogy a helyi érzéstelenítők kalciumszinergikusak.
A szövetekbe történő gyulladásos folyamat kialakulásának köszönhetően, amelyen helyi érzéstelenítőt adnak be, a nátriumcsatorna blokkolása a membrán külső felületén történik (5. ábra). Ugyanez a hatás figyelhető meg a membránreceptorok toxikus hatásaival szemben. Így lehetséges az akciós potenciál kifejlődésének számos szakaszát kiemelni, a helyi anesztetikumok hatására a szöveten:
- a receptorok kötődése a neurális membránban;
- a nátrium-ionok idegmembrán permeabilitásának csökkenése;
- a depolarizáció mértékének csökkenése, ami a küszöbérték blokkolásához vezet (a küszöbérték nem keletkezik);
- az akciós potenciál kifejlődésének megszüntetése, ami az impulzusjel blokádját eredményezi az idegben.
Mivel a helyi érzéstelenítő hatással van az idegrost membránjára, az injekció beadása után diffundál a kötőszövet különféle rétegei között.
Az érzéstelenítés koncentrációjának elegendőnek kell lennie ahhoz, hogy képes legyőzni a Ranver csomópontjait. A diffúzió legnagyobb nehézségei akkor merülnek fel, ha az epineurussal való érintkezés kapcsolódik. Az epineurium külső héja ideges "pajzsot" alkot, amely megbízhatóan védi az idegeket a külső hatásoktól. Körülbelül 5000 idegrost vesz részt a területnek
- mm. Mindezek a szerkezetek akadályt jelentenek, amikor az érzéstelenítő az idegrostra költözik. Az érzéstelenítő oldat megfelelő koncentrációja lehetővé teszi, hogy ne csak az idegrostra hatoljon át, hanem teljes blokádjának biztosítására is. A modern helyi érzéstelenítők segítségével ezt a célt elérheti anélkül, hogy megzavarná az ideg integritását vagy megsemmisítését.
Jelenleg az idegrostok blokádja három szakaszból áll:
- a fájdalom és a hőmérséklet-érzékenység kikapcsolása;
- kapcsolja ki a tapintást;
- a proprioceptív érzékenység letiltása és a motor impulzusok egyidejű vezetése; az izomlazítás kezdete.
Visszaállítása különböző érzékenység fordított sorrendben: először jelenik tetszőleges izomrángások és proprioceptív érzékelés, akkor helyreáll protopathic érzékenység és a legkevésbé - epicritic. Ebben az esetben, ha szükséges tartani a blokád ismételt injekcióval, egy új tétel érzéstelenítő oldatot táplálunk be egy idegtörzsben amikor fellendülés kezdődik funkcióit valamilyen külső szálak. A folyamat megy fordított irányban, és a blokád lehet elérni gyorsabban, kevesebb érzéstelenítő oldattal és alacsonyabb koncentrációban összehasonlítottuk a kezdeti.