Bookreader - víz (suslov b
3. Vízmolekula
Az emberi életben, mint bármely más lény életében, a víz óriási szerepet játszik. Az iváshoz és a főzéshez víz szükséges, mosáshoz szükséges víz szükséges. Hosszú ideig az ember rájött, hogy a víz szüksége van a mezejére. Ezért nem meglepő, hogy még az előttünk töltött évezredek előtt élt ősi népek is különös anyagként tekintettek a vízre, amely minden létező alapvető elve.
"A víz mint folyadék, mozgó, mindent átható, mindenben volt a kezdete" - mintegy két és fél ezer évvel ezelőtt tanították "a görög bölcs Thales of Miletus. Körülbelül kétszáz évvel később, Arisztotelész, az ősi világ legnagyobb filozófusa már több ilyen elsődleges alapot számolt be, a világ "alapvető elemeit", de közülük víz volt.
Az ókori görögök nyilatkozataiban, bármi legyen is ezek a kijelentések, most gyermeki módon naivak, már a víz jelentésének mély megértését tükrözték a természet és az emberi élet minden jelenségében.
Körülbelül 20 évszázad telt el. Az "elem" nagyon fogalma jelentősen megváltozott. A kémiai elemet egyszerű anyagnak tekintették, amelyet már nem lehet egyszerűbb anyagokká bontani. Az elemek száma nőtt és nőtt. Ezeknek az elemeknek a listája ismét víz volt.
És ennek oka volt. Végtére is, az akkori tudósok, különféle jelenségek figyelembevételével, amelyekben a víz részt vesz, soha nem vették észre, hogy kémiailag megváltozott. Előttük jégre keményedett, de a jég ugyanabban a vízben olvadt. A vizet felforraljuk, majd bepároljuk, hűtés közben a gőzök ismét csepp vizet kapnak. A víz mint anyag maradt "önmagában" minden folyamatban, és tekinthető egy elválaszthatatlan, egyszerű anyagnak.
A tizennyolcadik század végén csak egy fontos felfedezés volt, hogy a víz összetett anyag: a vizet mesterséges úton szerezték be, hidrogén gázzal oxigénnel égve. Ez bizonyította, hogy a víz hidrogénből és oxigénből áll.
Körülbelül ugyanabban az időben a víz összetett összetételét is fordítottan igazolta - a víz összetevőinek bomlása. Ezt a francia Lavoisier tudós végezte el. A piros forró fegyverhordón keresztül néhány vizet engedett. A magas hőmérséklet hatására a víz elbomlott. Az oxigént vassal kombinálták, és a hordó belső felületén megjelentek egy skála (vas-oxigén vegyület), és hidrogéngáz keletkezett a csomagtartóból.
Néhány évvel később a víz áramló árammal bontott fel alkotóelemeibe. Ily módon pontosan megállapították, hogy a vízben 11,11% hidrogén és 88,89% oxigén, és a hidrogén kétszer akkora térfogatú, mint az oxigén.
Ha mindkét elválasztott gáz keveredik, akkor szobahőmérsékleten ez a keverék nagyon hosszú ideig változatlan marad. A keveréknek csak egy hatodik része lett vízre, 54 milliárd évig kellene várnunk. De ha csak egy égő meccset hozsz ezzel a keverékkel, vagy átengeded az elektromos szikrát, kémiai reakció azonnal megtörténik az oxigén és a hidrogén között: a hidrogén ég el oxigénben, és ennek eredményeként víz keletkezik. Ezt a tapasztalatot nagy óvatossággal kell elvégezni, mivel az égést mindig nagy erõs robbanás kísérte. Ezért két térfogat hidrogén és egy térfogat oxigén keverékét csikorgó keveréknek nevezik.
Az oxigén és a hidrogén közötti reakció kialakulásához nem szükséges a teljes keveréket felmelegíteni. Elég, hogy a legkisebb mennyiséget melegítse. Ebben a kötetben elindul a hidrogén égési folyamata - az oxigénnel való kapcsolat. Ugyanakkor nagy mennyiségű hőt bocsátanak ki (tíz gramm robbanóanyag keverék elég nagy mennyiségű hőt termel az égés során, ami elég ahhoz, hogy csaknem fél liter vizet forraljon). A felszabaduló hőt átvisszük a keverék szomszédos részeire, és az égési folyamat rendkívüli gyorsasággal terjed a teljes térfogatban.
A lángoló láng hőmérséklete meghaladja a 3000 fokot. Ezért a robbanóanyagot autogén hegesztéshez is használják.
Tehát a víz összetett anyag, amely oxigénből és hidrogénből áll. Hogyan épül fel a vízmolekula? Melyek az oxigén és a hidrogén atomjai?
A modern tudomány van egy nagyon pontos vizsgálati módszerek, amelyek lehetővé teszik, hogy behatoljanak a szerkezet az anyag olyan mélyen, hogy még most mondhatjuk teljes bizonyossággal, hogy nemcsak ebből atomok állnak molekulák egyik vagy másik anyag, hanem arról, hogyan rendezett atomok molekulák . Mindegyik vízmolekula három atomból áll: egy atom oxigénből és két hidrogénatomból áll. Mind a három atom a molekulában úgy vannak elrendezve, hogy ha mentálisan kapcsolódni a sorokat, akkor egy egyenlő szárú háromszög képződik, amely háromszög, amelyben két oldal egyenlő (ábra. 3). A tetején egy oxigénatom van, és két sarkában a bázisnál - a hidrogénatomon. Az oxigénatom és a hidrogénatom közötti távolság azonos és 97 tíz milliárdos egy centiméternyi. A hidrogénatomok közötti távolság 154 tízmilliárdos egy centiméter, és a szög a csúcson, ahol az oxigénatom található, körülbelül 105 fok. Ha a molekulaméret tíz milliárdszor nő, akkor ez a háromszög egy közepes méretű asztalra illeszkedik.
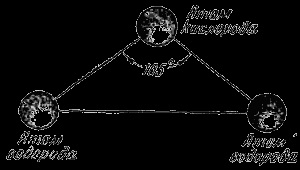
Ábra. 3. Az atomok elrendezése egy vízmolekulában.
Az olvasó megkérdezheti: Miért vannak a vízmolekula atomjai egy háromszög alakjában, és nem egy egyenes vonalban - egy oxigén atom közepén és a hidrogén atomjai szélein?
Ezt így magyarázhatja meg. Minden test természetesen a legstabilabb helyzetbe kerül. A sima tetőre dobott gömb nem marad lejtős felületén, és a gravitáció hatására szükségszerűen lefelé csúszik. Ha a kötélhez súlyt kötünk, és tartjuk a szálat a szabad véghez, akkor a súlyok meghúzzák a szálat, és pontosan a vízvezeték mentén helyezkednek el. A súlyokat kissé oldalra tesszük és felszabadítjuk - a súlyok nem maradnak az új instabil állapotban, és a gravitáció hatására gyorsan visszatér az eredeti pozícióba. Tehát egy molekula vízben. Az atomok egymáshoz kötődnek, amelyeket a kémiai affinitás erőinek neveznek. Ezen erők hatásának nagysága és iránya olyan, hogy a vízmolekula pontosan akkor stabil, amikor az atomok háromszöget alkotnak. Az atomok bármely más "konstrukciója" kevésbé stabil. És ha valamilyen oknál fogva az "atomok" elrendezése megváltozik, akkor az okok kiküszöbölése érdekében az atomok ugyanazt a háromszöget alkotják.
Meg kell mondani, hogy a hidrogénatomok és az oxigén atomjai a vízmolekulában nagyon nagy erõk. Nagyon nagy energia szükséges, úgyhogy az atomok közötti kapcsolat "felbomlik". 1400 fokos vízig melegíthetünk, és ezen a hőmérsékleten egy millió vízmolekulából csak mintegy száz molekulát bontunk hidrogénre és oxigénre. Még 3092 fokban is, minden vízmolekula 13 százaléka megsemmisül.
Minden víz, bárhol is vették - a Jeges-tenger, a mélyművelésű bányák Donbass, őrizetbe vették a hópehely vagy csillogott a kora reggeli harmatcseppek egy virág - a víz tagjai azonosan felépített molekulák. Azonban az egyes molekulák kölcsönös elrendezése egymáshoz képest folyékony vízben, hópehelyben vagy gőzkazánban lévő gőzben nem azonos.
A vízgőz, fűtött fokkal háromszáz, légköri nyomáson, hasonló a hagyományos gáz: amelyben közötti távolságok a molekulák elég nagy ahhoz, hogy minden egyes molekula létezhet többé-kevésbé független, anélkül, hogy olyan jelentős kölcsönhatás szomszédai, kivéve, természetesen azok Azokban az esetekben, amikor a véletlenszerű hőmozgás eredményeként létrejövő molekulák ütköznek egymással.
Hópehelyen vagy jégdarabon a molekulákat össze kell kötni és rögzíteni kell a kristályrács bizonyos helyein; A molekulák mozgása a többségben csak bizonyos pontok körüli oszcillációra korlátozódik.
És hogyan vannak a molekulák a folyékony vízben?
A tudományban még mindig nincs szigorú, szilárdan megalapozott elmélet, amely a folyadékok szerkezetére, különösen a vízre vonatkozik. Feltételezzük, hogy a folyékony víz szerkezete valami a jégkristályok és a gőz között. Tanulmány a víz szerkezetét infravörös és röntgen lehetővé tette, hogy feltételezzük, hogy közeli hőmérsékleten fagypont, a folyadék molekulái víz gyűlik össze kis csoportokban, és „csomagolt” egy térben megközelítőleg olyan kristályok alakjában, és a közeli hőmérsékleteken a forráspont víz, normális nyomáson, szabadabban helyezkednek el, véletlenszerűen. Azonban a "keret", amely folyékony vízben egyes molekulákból áll, nagyon rugalmasnak kell lennie. Ellenkező esetben nehéz lenne megmagyarázni a víz mozgékonyságát, annak a képességét, hogy "működő szervezet" legyen, amely nehéz turbina kereket vezet, és különböző tápanyagokat szállít az élő szervezetek legfinomabb hajói számára.
Nyilvánvaló, hogy még a vízgőzben is alacsony hőmérsékleten egyes vízmolekulák kombinálódnak, vagy ahogyan azt mondják, társulnak.
A víz a leggyakoribb folyadék a természetben. Annyira megszoktuk a vizet, annak különböző megnyilvánulásait, hogy számunkra a legegyszerűbb folyadék. A víz számos tulajdonsága mérési rendszerünk alapja. A jég olvadási hőmérsékletét nulla foknak tekintjük, és a forráspont száz fok (a Celsius skála szerint ma már szinte mindenütt elfogadott). Egy köbméter térfogatú víz tömege a tömeg tömegének egy grammja. A hőmennyiség, amely egy fokban felmelegszik egy gramm vizet, a hő kalóriatartalmát nevezzük. A fizikusok és a vegyészek mérőeszközei vízen végzettek, és a más anyagokra mért értékeket általában a vízhez kapott számokkal hasonlítják össze. De ha jobban megnézed, hogy a viselkedést a víz különböző körülmények között és hasonlítsa össze a viselkedését a legtöbb más folyadékok, azt látjuk, hogy a „rendes” folyékony viselkedik, nagyon furcsa, ha ezek a szavak kifejezik a sajátos jellegét a víz, élesen megkülönbözteti minden más folyadékok .
Most a víz egyik legfontosabb és érdekes tulajdonságáról beszélünk, és eltérnek a folyadékok viselkedésének általános "szabályaitól".