A kén (ek), a képlet és a példák móltömege
A kén egy kémiai elem, amely a periódusos rendszer VIA csoportjának harmadik szakaszában található. Mendelejev Egyetem.
A rendszám 16. Az atom szerkezete az 1. ábrán látható. 1. A p-család nemfémje.
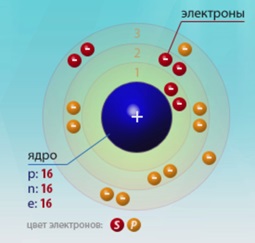
Ábra. 1. A kénatom szerkezetének ábrája.
Normális körülmények között, a kén egy törékeny sárga olvadó kristályok hőmérsékleten 112,8 o C Sűrűség 2,07 g / cm 3. vízben oldhatatlanok, de elég jól oldódik szén-diszulfid, a benzol és más folyadékok. Elpárologtatására folyékony kén ki az oldatból, mint egy átlátszó sárga rombos rendszerben kristályok alakja octahedrons (rombos módosítás).
Ha az olvadt kén lassan lehűtjük, és akkor, amikor azt részlegesen vulkanizált összevonni még nem volt ideje, hogy megnehezítse a folyadék kap egy hosszú, sötét sárga tűszerű kristályok monoklin rendszer (monoklin módosítás). Sűrűség 1,96 g / cm 3. Az olvadáspont 119,3 ° C.
A kén móltömege 32,065 g / mol. Ez az érték azt jelöli, hogy az anyag (m) tömege az (n) anyag móljainak számával M-vel jelölt, és a következő képlet segítségével számítható ki:
Más szóval, a moláris tömege az anyag - a súlya 1 mol az anyag, g / mol vagy kkmol.
Mivel, függetlenül attól, módosítás kén a szilárd vagy folyékony halmazállapotú, de nem a gáz, hogy megtalálják a értéke a molekulatömeg nem tudja használni az érték a moláris mennyiség, vagy a számítások az alábbi képlet segítségével Mengyelejev-Clapeyron.
Példák a problémamegoldásra
Mekkora a kén tömege, amely alumínium-szulfid Al2 S3 előállításához 30 g tömegű? Milyen feltételek mellett lehet ilyen szulfidot egyszerű anyagokból előállítani?
Tegyük fel a kén-szulfid előállítására szolgáló reakció egyenletét:
Az alumínium-szulfid anyag mennyiségét (moláris tömege: 150 g / mol) számítjuk:
Az n (Al2S3) reakcióegyenlet szerint. n (S) = 1: 3, akkor:
n (S) = 3 × 0,2 = 0,6 mol.
Ezután a kén tömege egyenlő lesz (moláris tömeg - 32 g / mol):
m (S) = n (S) x M (S);
m (S) = 0,6 × 32 = 19,2 g.