Vosevi (vosevi) - az USA-ban engedélyezett hepatitis kezelésre szolgáló új gyógyszer
A szerkezet a regisztrált gyógyszerekből sofosbuvir. velpatasvir és egy új kapcsolat - voksilaprevir. Voksilaprevir egy proteáz inhibitor 3 / 4A. A minisztérium azt mondta, hogy Vosevi lett az első gyógyszer jóváhagyott betegek kezelésére, akiknek esett át terápia sofosbuvir vagy más anti-hepatitis gátló gyógyszerek NS5A.
Kombinált készítmény használatát foglalja magában egy alkalommal naponta, minden tabletta 400 mg sofosbuvir, 100 mg-os és 100 mg-os velpatasvira voksilaprevira. Gilead meghatározott ár Vosevi 24 $ 920 per csomag 28 tablettát kiegyenlítse a Epclusa, tabletta, amely tartalmaz 400 mg sofosbuvir, velpatasvira 100 mg (74 $ 760 a 12-hetes), azaz Gilead valójában egy harmadik komponens Vosevi ingyen. Kombinációs terápia engedélyezett újbóli hepatitis C vírus (HCV), az előző hiba terápiás rezsimek minden genotípus alapján NS5A inhibitorok, valamint a kezelés sikertelensége 1a genotípusú vagy 3, ahol az előzőleg használt üzemmód alapú sfosbuvaira nélkül NS5A inhibitorok.
A POLARIS sorozat III. Fázisának legfontosabb klinikai vizsgálataiban a 12 hetes Vosevi-kezelés hatékonyságát és biztonságosságát vizsgálták a cirrózis nélküli vagy a közvetlenül ható hatású gyógyszerekkel korábban kezelt májkárosodásban szenvedő betegeknél.
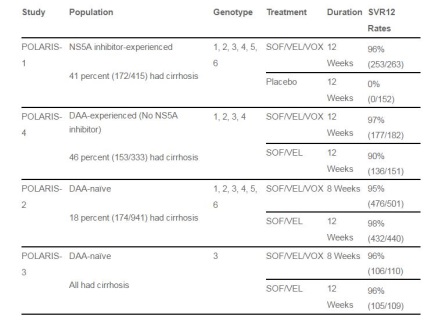
Study POLARIS-1 hatást mutattak 12-hetes kezelés Vosevi 96,2% (elérése tartós virológiai válasz 12 héttel a terápia befejezése után, SVR12) betegek (n = 263), a korábban poluchavih módok alapján NS5A inhibitorok. Egy hat vizsgálat során a betegek szignifikáns rezisztencia mutációk.
A tanulmány POLARIS-4 hármas kombinációs Vosevi (n = 181) hasonlítjuk össze a kezelés sofosbuvir és velpatasvirom (n = 151) betegeknél cirrhosis és anélkül cirrhosis korábban kezelt módok alapján sofosbuvir használata nélkül NS5A és NS3-inhibitorok szintén nem tartoznak kapó betegeknél klasszikus interferon kezelést ribavirinnel. Triple mód SVR12 előírt esetek 98% -ában, míg a 90% esetében a kettős módot.
A Vosevi toleranciája nagyon magas volt, és durván megfelelt a placebo csoport tolerálhatóságának. A leggyakoribb fejfájás, fáradtság, hasmenés és émelygés.
Korábban az FDA jóváhagyta a cofosbuvir + velpatasvir (NS5B RNS polimeráz inhibitor) kombinációját. A kombinált gyógyszer hatékonyságát és biztonságosságát a III. Fázis több klinikai vizsgálatának eredményei is megerősítették, amelyekben hepatitis C és májcirrhosis (vagy anélkül) részt vettek. A kapott eredmények szerint 12 hétig egy új gyógyszerrel végzett kezelés után a vírus 95-99% -a leállt a vérben.