Nizkomolekulyanyh vegyületek kölcsönhatása membránok - elvont, 5. oldal
Egyértékű ionok, mint például a nátrium, sőt con-zyvayuetsya savas foszfolipidek, de kis affinitású.
Igaz affinitása Ca 2+ a felszínre ikerionos foszfolipid vezikulák közelében, vagy valamivel kisebb, mint a felszínen a savas foszfolipidek. Erősebben kötődik a Ca 2+ savas foszfolipidek okozott nem bblshim affinitása ehhez Ca 2+. és az elektrosztatikus hatás valószínűleg nagyobb sűrűségű negatív töltések, amelyek növekedéséhez vezet a helyi koncentrációja a Ca 2+ a felületen.
A kötés egyszeres és kétértékű kationok, látszólag csekély hatása van az Aa poláris fej foszfolipidek, legalább foszfatidil-kolint és foszfatidil-glicerin. Való kötődés foszfatidil megfigyelt immobilizálására karboxilcsoportok.
Jellemzően, Ca 2+ kötődik a foszfolipideket sztöchiometriája 1: 1, bár abban az esetben, foszfatidil-kolin egy Ca 2+ iont kötődik két molekula lipid. Úgy tűnik, a képződött komplex, és a sztöchiometriai 1: 2, ennek eredményeként a fém kötés bekövetkezik aggregáció membránok; ahol a kétértékű kation szolgálhat egy híd két szorosan nyomni felületei a membrán.
Kötődése Ca 2+ vezethet a változás a fizikai állapota a lipid. Például, a kötési Ca 2+ foszfatidil vagy foszfatidsav kísérheti a fázisátmenet kétrétegű gél, és a kölcsönhatás a ct-diolipinom stabilizált hexagonális fázis. Ha a vezikulumok keveréke savas és ikerionos lipidek, a kötődését Ca 2+ okoz oldalirányú fázisszétválást; így képezhetnek széles körű domének unilamelláris vezikulumok.
Annak előnyeit ad kötési foszfolipidek Mn 2+. mert a paramágneses ion megváltoztatja terjedhet 31P-NMR. Ezek a változások függenek helyi koncentrációja Mn 2+, és így fel lehet használni mérésére felületi potenciál.
A savas kettősrétegek felületkezelt szilárdan ráöntött például a polikationok, azaz például poli- vagy gentamicin.
Zeta potenciál és elektrokinetikus jelenségek
Ha hólyagocskák helyezünk egy elektromos mező, akkor elmozdulni az elektróda, olyan díjat, amely szemben van a jele, hogy az felelős a vezikulum. Elektroforetikus mozgékonyság-lic vezikulumok meghatározva ún zéta poteitsialom amely egyenlő közötti potenciál az oldat térfogatát, és az úgynevezett Helmholtz síkjával párhuzamos a membrán síkjában. Ez a sík elválasztja a vastag része a kettős elektromos réteg, ami mozog az elektromos mező együtt a membrán és tároljuk körülbelül 2 A töltött vezikulum felületén. Így, a nagysága a zéta potenciál kisebb, mint az érték a felületi potenciál, és a felületi potenciál kapcsolódik az arány által meghatározott elméleti Gouy - Chapman. Mérése a zéta potenciál rejlik az alapja az egyik a standard értékelési módszerek a felületi potenciál, és fel lehet használni, hogy tanulmányozza a kötődését ionok a felülettel foszfolipid veznkul. Az elektroforetikus mobilitás szintén befolyásolják a jelenlévő kiálló felszíne fölé a töltött kétrétegű Neelie Pydna-membrán alkotóelemeket, mint például fehérjék vagy gangliozi-sorok és használata elektrokinetikus technikáktól kaphatnak néhány információt a megoszlása a díjak a felszín közelében a vezikulumok.
Hidrofób kötésen ionok és membrán reagenst
A jelenléte felületi potenciál hatással lehet a kötődés a hidrofób membrán felületének és amfifil ion-TION membrán reagenst. Ez lehetővé teszi, hogy néhány, a próbák a felületi potenciál mutatókat. Ábra. 7.9 ábra a szerkezeti képletek bizonyos próbák. Mindezen vegyületek, a spektrális jel intenzitása korrelációban lehet a próba mennyiségét a membránhoz kötődik, és ezért a felületi potenciál értékét. Az ilyen próbák tanulmányozására használnak sok töltésű foszfolipid vezikulák
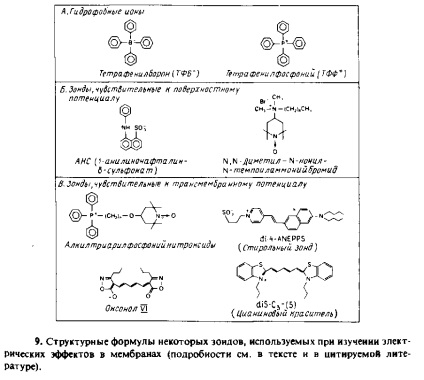
Vizsgálat használja őket Biomembranes problematikusabb, mint a spektrális jellemzői a szonda függhet nem csak a felületi potenciál, hanem a pH-vagy a membránpotenciál, ami nagyban megnehezíti az értelmezése a megfigyelt spektrális változásokat. Példaként a ANS kötődés mitokondriumok, és a változás a spektrális jellemzőinek neutrálvörös történő kötődés szubmitokondriális részecskék.
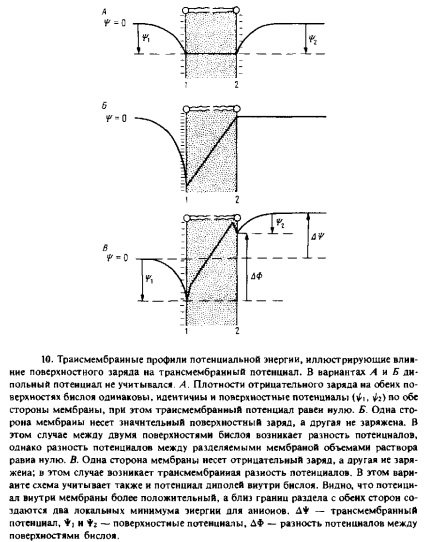
Ábra. 7.10, A azt mutatja, a profil a villamos potenciál, hogy a membrán mindkét felületét, amelyek negatív töltésű. A jelenlétében a membrán felületi potenciál növekszik a koncentrációja Ezen membrán hidrofób kationok, mint a TPP + vagy K + -valinomitsin komplex. Ez annak a ténynek köszönhető, hogy a helyi koncentrációja ionok a felszín közelében a membrán nagyobb, mint a hatóanyag koncentrációja az ömlesztve. Emlékezzünk, hogy a permeabilitási együttható ábrázolható, mint a termék a eloszlási koefficiens / 3 állandó mozgási sebességét az ion a membránon keresztül a, így, mert a nagy mennyiségben / 3 negatív töltésű membrán permeabilitás hidrofób kationok nagyobb, mint a töltés nélküli. A függőség a vezetőképessége a membrán felületi töltés kielégítően egyenletben leírt Gouy-Chapman felületi potenciál.
Megjegyezzük, hogy a lehetséges belső dipólusok befolyásolhatja mind a kötődését a hidrofób ionok a felszínen a kettős réteg, és a sebességi állandó transzmembrántranszportot, míg a hatás a felületi potenciál szimmetrikus permeabilitása miatt kizárólag annak hatását a eloszlási koefficiens. Abban az esetben, aszimmetrikus eloszlása felületi töltések, a helyzet bonyolult. Az ilyen aszimmetrikus eloszlása a lipidek - jelenség egyáltalán nem ritka. Ebben az esetben, a jelenlegi a membránon keresztül potenciálgradiens hátráltatja a átadását kationok a vizes fázisból 1 2. fázis, és elősegítik az kationok az ellenkező irányba.
4. A transzmembrán potenciál
A transzmembrán potenciál definíció az elektromos potenciál közötti különbség két vizes fázist elválasztjuk membrán. Közötti kommunikáció a transzmembrán potenciál és a felületi potenciál * i és r ♦ grafikusan ábrán látható. 7.10 A A diagram azt mutatja, hogy a potenciális különbség a két felület DF membrán eltérhet L * miatt az aszimmetrikus töltéseloszlás a két felület között a kettős réteg. Bármilyen membrán belsejében található töltésű csoportot fog mozogni a helyszínen DF potenciállal. D * is nevezik maradék potenciál, és ez ezt az értéket, ha ez lehetséges, mért elektróda pár.
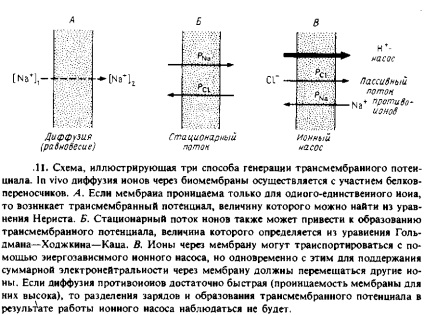
Hozzon létre egy transzmembrán potenciál több szempontból is. Vázlatosan vannak ábrán mutatjuk be. 7.11.
1. Egyensúlyi körülmények között. Ha a membrán permeábilis semmilyen konkrét ion, például Na +. és átjárhatatlan másoknak, akkor lehet, hogy egy diffúziós potenciál, amely arányos a logaritmusát koncentrációk arányát ionok áthatoló egyik és a másik oldalon a membrán. A diffúziós az ion a membránon keresztül, majd egy transzmembrán töltés szeparáció és így létrehozott potenciális különbség megakadályozza a további diffúzió. A töltést kell mozgatni a membránon keresztül, hogy hozzon létre rajta egy adott értéket ABA, ki lehet számítani a membrán kapacitása. Ahhoz, hogy hozzon létre egy L * = 100 mV kell mozogni egy töltéssel 250 foszfolipid molekulák. Egyértelmű, hogy a felületi töltés sűrűség egyidejűleg változik nagyon kicsit.
Az egyensúlyban, D * határozza meg a Nernst-egyenlet:
Ugyanez egyenletet lehet használni abban az esetben, ion transzfer vegyértékének Z. Biomembranes permeabilitás ionok kapcsolatos működésének specifikus ioncsatornák. Meg lehet mesterségesen megnövelték specifikus ionofórokkal vagy ion hordozók, mint például a K + valil-nomitsina.
Álló diffúzió ion áram. Ha a membrán áteresztő dyal néhány ionok fognak mozogni rajta. Az egyensúlyi állapotban különbségek miatt a permeabilitási együtthatót a különböző ionok lehet egy transzmembrán potenciál különbség. Más szóval, a töltés szeparáció a membrán egy ilyen helyzetben lenne annak a ténynek köszönhető, hogy egyes ionok diffundálnak a membránon keresztül gyorsabb, mint a másik. A leíró egyenlet ez a helyzet, az úgynevezett egyenlet a Goldman-Hodgkin-Katz és abban az esetben két ion a következő:
Az ionok mozgását addig folytatódik, amíg ezután, amíg egyensúly jön létre.
Aktív transzport ionok. A transzmembrán töltés szeparáció is előfordulhat az aktív transzport folyamatok. Sok enzim katalizálja reakciót társított költség transzfer vektor keresztül a kétrétegű. A példákban különböző ATP-függő ionpumpák, így például Ca2 + -ATP-áz aktivitás vagy citokróm c-oxidáz, amely egy proton pumpa. Itt megjegyezzük, hogy ezek csak az enzimek által katalizált reakciók elektrogén, t. E. kíséri át a díjakat a kétrétegű. Nyilvánvaló, hogy egy ilyen rendszer ott kell lennie valamilyen semlegesítő transzmembrán ion fluxus. A ábrán látható rendszer. 7.11, olyan áramlási egy passzív kontrtransport ion
Ez akkor fordul elő, amikor a protonpumpa. Mint abban az esetben a passzív ionáramlással, számláló áramlási sebesség kisebb lesz, mint a sebesség az aktív folyamat, és ennek eredményeként a teljes fluxus ionok révén a kettős réteg nem lesz elektromosan semleges, és a membránpotenciál különbségek keletkezik №. Ha a kettős réteg áteresztőképessége semlegesítő ionokat, hogy elég nagy, a töltés szeparáció fognak tűnni. Ezt az elvet alapul használata ionoforokkal, hogy megszüntesse a transzmembrán elektromos potenciál létrehozott biológiai membránok és modell rendszerekben.