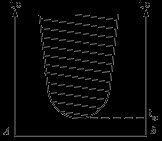
Imost összetétele a gőzfázis hőmérsékletének
Növekvő hőmérséklettel a gőz az egyensúly az illékony elegyét állandó összetételű feldúsul a komponens, részleges moláris párolgási hő nagyobb. Ez a törvény érvényes illékony vegyületeket, például nélkül azeotropot és azeotrópot.
Ahogy a hőmérséklet növekszik a rendszerben a nyomás görbe max gőz egyensúlyi gőz összetétele és az összetétele az azeotrop keverék változik ugyanabba az irányba. Egy rendszer m és egyensúlyi gőz összetétele az azeotrop keverék változik ellentétes irányban.
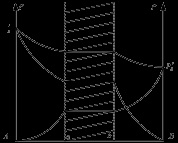
Sok folyadékok korlátozott kölcsönös oldhatóságot és egy bizonyos hőmérséklet-tartományban, és összetétele keverve formák 2 fázis. Például, anilin - víz: AB - jellemzi a változás anilint vízben való oldhatósága a hőmérséklet-változásnak. BC - leírja a változás vízben való oldhatósága a változása anilin T. AB és BC találkozik a B pont az úgynevezett felső kritikus oldhatósági hőmérséklet. Ezen hőmérséklet felett a folyadékok térfogatának vegyes bármilyen arányban. Ha a HOLD izotermát, hogy átlépi a görbe ABC, akkor át egy pont és egy, és a kettő kombinációjának a vizes réteget, és - az összetétele a anilin-réteg. Megoldások megfelelő a készítmény A pont és a B azt mondják, hogy konjugátum, és az úgynevezett csomóponti az AB szakasz. Ha vesszük az elegyet az anilin és víz összetételű talicska d és melegítsük ezt a keveréket olyan hőmérsékletre, látni fogjuk, az üvegfázis 2: 1) vizes oldatát d1, és a másik réteg az anilin. Súlyok fázis konjugátum megoldásokat lehet meghatározni a kar szabályt. Ahhoz, hogy megtalálja a kritikus oldhatósági hőmérséklet alkalmazható általában négyszögletű átmérője.
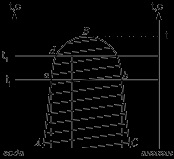
5.Davlenie telített gőz egy korlátozott kölcsönös a komponensek oldhatósági a rendszer
Az ilyen rendszerekben vizsgáltuk, mind a folyékony filmréteg ugyanolyan gőz (összetételét és teljes nyomás a parciális nyomás a C komponens) egyensúlyi állapotban.
A különbség a teljes folyadék heterogén régió korlátozó eszköz egyetlen különbség relatív mennyisége a két réteg állandó összetételű egyes. Mint egy általános és parciális gőznyomása az egész említett területen tárolja konstans értékek.
6.Vzaimno oldhatatlan folyékony
Ha folyékony kölcsönösen oldhatatlan,, alkotnak heterogén rendszer, amelyben minden egyes komponens függetlenül létezik a másik. A gőznyomás az egyes komponensek a keverék egyenlő a nyomás a tiszta komponens gőz.
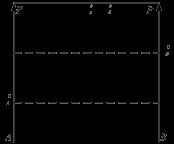
A teljes gőznyomása a keverék kölcsönösen oldhatatlan folyadékok az összege gőznyomás a tiszta komponensek ugyanazon a hőmérsékleten. Ezért, az ilyen keverékek forraljuk hőmérsékleten alacsonyabb, mint a forráspontja az egyes komponensek. Amint a párolgás a heterogén keveréke forráspontja hőmérséklet állandó marad, amíg teljesen elpárolog egyik összetevője a rendszer után a forráspont hirtelen változik a forráspontja a fennmaradó komponense. Ezt használják a szakterületen, és laboratóriumi gyakorlat vízgőzdesztillációval. Összetétel gőz nem függ a komponensek aránya a folyadék. és jelző móljainak a száma a komponens, A és B páros és nyert gőz kondenzátum. Ha - V pár, az egyenlet Mend-Clap lehet rögzíteni. Ha a második komponens vízgőz to.- fogyasztható együttható. Ő nagyobb, mint kisebb. Vízgőz-desztilláció eltávolítására használják benzol kőszénkátrány, tisztítás anilin.