Fiziko-kémiai tulajdonságok a fehérjék
A legtöbb hidrofil fehérjék. Azonban, a fehérje molekulák nagyon nagy, így a fehérjék nem képeznek valódi oldatokat és a kolloid csak. A külső megnyilvánulása e - ez Tyndall-jelenség (vagy Tyndall kúp). Tyndall szóródási hatás okozza a vékony fénysugár halad át a fehérje-oldatot. Annak ellenére, hogy nagy mennyiségű, számos fehérje molekulák nem csapódik vizes oldatokban. Csapadék a fehérje molekulák gátolják faktorok stabilizálására fehérje oldat.
Tényezők stabilizáló protein oldatban.
Hidratálás héj - egy réteg vízmolekulák orientált egy bizonyos módon, hogy a felület a fehérjemolekula. A felület a legtöbb fehérje molekulák, negatív töltésű, és a dipólusok vízmolekulák vonzódnak hozzá annak pozitívan töltött pólus (lásd az ábrát).
B
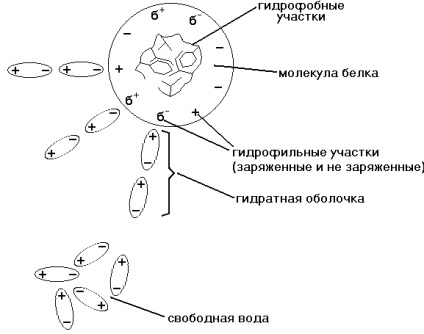
Tulajdonságok hidrátvíztől shell
a) A forráspont feletti 100 0 C-on
b) a fagyasztási hőmérséklet 0 ° C alatt
c) A vízben oldhatatlan hidratációs héj különböző sókat és egyéb hidrofil anyagok.
g) körülveszi az egyes fehérjemolekula hidrátburok teszi ezt a fehérjemolekulák megközelíteni, és csatlakoztassa kicsapódni.
2) a felelős a fehérje molekulák. A felület a legtöbb fehérje molekulák van töltve úgy, hogy minden fehérjemolekula van egy szabad feltöltött COO - és NH3 + csoport. Az izoelektromos pont (IEP) a legtöbb fehérje a test egy gyengén savas közegben. Ez azt jelenti, hogy az összeg az ilyen fehérjék sav (COOH) csoportban nagyobb, mint a számos alapvető csoportok (NH3). pH-ja a vérplazmában körülbelül 7,36 - magasabb pl legtöbb fehérje, így a plazma proteinek negatív töltésű.
Módszerek a fehérje kicsapódását
Két csoportra oszthatók:
1) módszerei lerakódása a natív fehérje
2) leválasztási eljárásokkal denaturált fehérje
Ahhoz, hogy kicsapjuk a fehérjét, az oldatból, szükséges megfossza azt mindkét faktor stabilizálására: mind töltésre, mind hidratációs héj.
A lerakódását natív fehérjék
Ahhoz, hogy a natív fehérje molekulát, töltését meg lehet szüntetni egyetlen módja annak, hogy a pH-t az izoelektromos pontra a protein (pI), és a legtöbb fehérje a test PI gyengén savas közegben. Tovább stabilizáló tényező - hidratációs héj eltávolítható, különböző módokon.
A legjellemzőbb példa natív fehérje kicsapódását kisózással.
a) sózás - egy fehérje kicsapás nagy koncentrációban, semleges sók, alkáli- és alkáliföldfém-sók, mint például a hidrofil és igen magas koncentrációban dehidratáló tulajdonságok. Leggyakrabban ez NaCl, Na 2SO 4. (NH4) 2SO 4. CaCl2. Azáltal, mint például a só, hogy az oldat a fehérje azokat eredetileg szabad vízben oldva, majd, a további növekedés a sókoncentráció, versenyben a fehérje a birtokában a víz, amely része a hidratálási kagyló. Kevesebb hidrofil proteinek, amelyek rosszul megtartja vízkötő shell elveszíteni előtt. Több hidrofil proteinek igényel a nagyobb sókoncentráció sózására. Ezért, a kisózás lehet elválasztott fehérjéket különböző mértékű hidrofilitás. Ily módon, például, lehet osztani albuminok és globulinok a vérplazmában.
Amikor sózás konzervált natív fehérje molekulák. Ha proteint kicsap keresztül kisózással, majd csökkentse a sókoncentráció, például dialízissel, a fehérje ismét feloldódik.
Fehérjekicsapássai elvesztése nélkül natív állapotát is érjük el vízelvonó szerek.
b) a használata egy dehidratálószer. Az ilyen szerek olyan oldószerek, amelyek vízzel elegyednek bármilyen arányban. A legtöbb esetben az aceton, etil-alkohol. Ezek az anyagok fogyasztása hidrát burokfehérjék, majd a proteineket kicsapjuk, ha töltés nélküli. De, ellentétben a kisózási, a csapadékot egyszer (egyszer!) El kell választani az oldószert. Ha az oldószer és a fehérjét, hogy állandóan érintkezésbe, hogy előfordulhat visszafordíthatatlan változások a fehérje szerkezetének a molekula (denaturáló).