Értékelése az elektron sűrűség eloszlása a molekulák a org-in
Vegyérték-állapotú atomok ugleroda.Obrazovanie kapcsolatokat.
C-atommal tölteni 6 m.
Az utolsó energia szinten tartalmaz 4 szénatomos elektron, melyek közül kettő elfoglalni 2S- orbitális gömb alakú, és a két elektron elfoglalják 2p pályák amelynek gantelepodobnuyu alakja. Gerjesztés hatására elektron a 2s-orbitális válthat egyik üres 2p-pályák. Ez az átmenet igényel energia költség (403 kJ / mól). Ennek eredményeként a gerjesztett szénatom négy párosítatlan elektront és elektron konfiguráció által kifejezett 1 2s 3 2p általános képletű
Excited szén: 1s22s12px12py12pz1
Hibridizálás - a jelenség a kölcsönhatás, I m \ egy molekulapályák szoros az energia, és amelynek közös elemei a szimmetria, a MOD-em hibrid pályák az alacsonyabb energia.
sp3-hibridizációs (1 vegyértékállapota szén), azzal jellemezve, homológ sor metán.
Kémiai kötések felmerülő metán m \ y darab szénatomot tartalmazó, és hidrogén viszonyítva típusú Xia # 948; -kötéseken (SP 3 -s-kötés). # 963; m -bond \ y szénatomot és hidrogénatomot ARR-HN hibrid sp3-szén és hidrogén felhők felhők. A fő különbség # 963; -kötéseken másoktól, hogy az átfedés a pályák impl Xia mentén összekötő vonal az atommagba.
sp2-hibridizáció (vegyértékállapota 2 szénatomot tartalmazó) mod-Xia-a kölcsönhatás és két p pályák (Px és Py), és az S-orbitális, és képződött sp2-pályák egy síkban fekszik, és a MOD-m szöge 120 °. Jellemző-ben a homológ sor etilén.
A kettős kötés-mod a sp2 hibridizált pályák, és a p-mod-linket nem-hibridizált p pályák.
SP-hibridizáció (3 vegyérték állapotban szénatomos) mod-Xia-a kölcsönhatásban, és s-pályák px-orbitális.
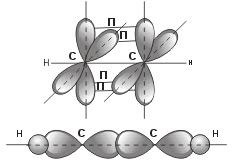
SP-hibridizáció a jellemző a lineáris orientációja a molekulapályák. Har-on egy homológja a második sorban acetilén. # 963; -bond MOD-hibrid szén SP-felhő az ugyanabban a síkban, és a négy p-elektron felhő mod p két-T-kapcsolat egymásra merőleges síkban.
Értékelése az elektron sűrűség eloszlása a molekulák a org-in. Módszerek átvitelére elektronikus vldiyaniya atomok.
Minden alkatrész a molekula atomot nach-Hsia a kapcsolat és a kölcsönös befolyás tapasztalat. Ez a hatás főleg továbbított, h \ s rendszer kovalens kötést pom \ nd úgynevezett Elektronikus effektov.Elektronnymi hatások úgynevezett elmozdulása az elektronsűrűség az állítólag-les befolyásolja képviselők.
Atomot poláris kötés, részleges díjat jelöli a görög betű „delta” (# 948;). Az elmozdulás az elektron-sűrűség a lánc egyszerű C-C kötések nevezett Xia induktív hatást, és jelöljük az I.
Induktív hatás átadódik az áramkör csillapító. eltolási irányban az elektron sűrűsége s -kötéseken jelzett egyenes nyilak.
Az öt-attól függ, hogy az elektron sűrűséget távolítva venni egy szénatomon vagy közel hozzá, az úgynevezett negatív indukciós hatásának (-I), illetve pozitív (+ I). A jel és nagysága az induktív hatás, határozza meg a különbségeket figyelembe vett elektronegativitási szénatom között, és a csoport, annak a hívó fél.
Atom „halogató” e-s-kötési sűrűség a saját oldalán, szerez egy negatív töltés # 948; -. Ha figyelembe vesszük atom párokat kovalens kötés, egy elektronegatív atommal, az atomok halogató nevezett oldott-akceptor. ez negatív induktív hatást. Társa az s-kötés, illetve lesz egyenlő nagyságú az elektronsűrűség a hiány, azaz részleges pozitív töltés # 948 + lesz az úgynevezett Xia donor. Ez egy pozitív indukciós hatása.
+I-hatás mutatnak alifás szénhidrogéncsoportok, azaz alkilcsoportok (metil, etil, stb). A legtöbb funkciós csoportok mutatnak -I-hatás: halogén-, amino-, hidroxil-, karbonil-, karboxil-csoport.
Induktív hatása megnyilvánul, ha a kapcsolódó szénatomok megkülönböztetve hibridizáció.
Hatása szubsztituensek az elektron sűrűség eloszlását az átvitt p-kapcsolatok, úgynevezett mezomer hatékonyságát-mennyiség (M). Mezomorf hatása is pozitív vagy negatív. A szerkezeti képletekben ábrázolják ívelt nyíl kezdve a központ a elektronsűrűség és befejezve a ponton, ahol az elektron sűrűség eltolódik.
A párosítás a jelenség-ARR-ed-elektron felhő, összesen 3 vagy több szénatomos.
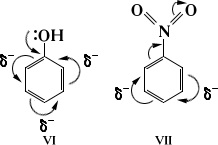
Szabad elektronikus hatások újraelosztását eredményezi a elektronsűrűség a molekulában, és a megjelenése részleges hajnal-Ing egyéni atomok. Ez határozza meg a molekulák reakcióképességének a.