Karbonsav (2 óra) tartalom platform
1. Definíció. Minősítést.
2. izoméria és nevezéktana monokarbonsavak
3. Fizikai tulajdonságok savak
4. Kémiai tulajdonságok. Szerkezete a karbonilcsoport.
A karbonsav - egy szénhidrogén-származékok, amelyek egy karboxilcsoportot (-COOH).
Osztályozása karbonsavak
Karbonsavak szerint osztályozzák két szerkezeti jellemzőit.
1) száma szerint a karbonsav-csoportok vannak osztva:
Ø egyértékű (egybázisú)
Ø több bázisú (dikarbonsav, trikarbonsav és t. D.)
2) A természet a szénhidrogéncsoport megkülönböztetni sav:
Ø limit (például, CH3CH2CH2COOH)
Ø telítetlen (CH2 = CHCH2COOH)
Ø aromás (RC6H4COOH)
Korlátozása egybázisú karbonsav
Az általános képlet az ilyen savak - CnH2nO2 vagy CnH2n + 1COOH
Nómenklatúra és izoméria karbonsav
A savak, amelyek kevesebb, mint négy szénatomot tartalmazó izomerek. Ha a szám egyenlő a négy atom, a sav két izomer, kivéve, ha a száma atomok, öt - öt izomerek.
Hogy típusú savak, az alábbi nómenklatúra:
Nevek épített karbonsavak alkalmazásával, mint az alap neve ecetsav. Mások minősülnek-származékok helyettesítéssel a hidrogénatomok a metil-csoport a bonyolultabb gyökök. Más szabályok teljes mértékben megfelelnek a szabályoknak a racionális nómenklatúra szénhidrogének (részletek meghatározott elején az előadás során).
Elkészítésekor a cím szerinti karbonsavat kapunk alapját figyelembe a leghosszabb lánc, beleértve a karboxil-csoport. Számozás kezdődik a karboxil-csoport a szénatom (a szám jelzi a helyzetét a funkciós csoportok, amelyek nem adnak). Ahhoz, hogy a név a szénhidrogén a szénatomok száma a fő láncban hozzáadott utótag -ovaya savat. Számok és előtagok azt jelzik, a helyzetét és számát szubsztituensek.
Nómenklatúra nómenklatúrája karbonsavak azonos aldehidek. ami nagyban megkönnyíti a megértést és a tanulást.
Nevei egyes képviselői karbonsavak
Előállítása karbonsavak
Számos eljárás előállítására egybázisú savak figyelembe vették az előző fejezetekben:
1) Alkoholok oxidálására
2) ozonolízis alkének
3) oxidációja a karbonilvegyületek (aldehidek és ketonok)
4) hidrolízisét a geminális trigalogenproizvodnyh szénhidrogének (hasonló hidrolízis digalogenproizvodnyh megszerzésében aldehidek módszer 5):
5) hidrolizáljuk-származékok (halogénezett származékai, észterek, nitrilek)
6) szénsavas fémorganikus vegyületek
Ez egy sokoldalú előállítására szolgáló eljárás karbonsavak, olyan laboratóriumi módszer.
Alsó sav, amelynek C1-C3 alkilcsoport - színtelen folyadék, jellegzetes, átható szag.
-Összetétele a C4-C9 - egy olajos folyadék, kellemetlen szag, rosszul oldódik vízben.
-Összetétele C10 és a magasabb - szilárd anyagok nem oldódnak vízben.
Így, a molekulatömeg növekedésével savak a vízben való oldhatósága csökken.
Magas hőmérsékletű forrásban levő sav képződése okozza az intermolekuláris hidrogénkötések van összekötve ezt, és jól oldódnak vízben (a hidrogén kötések kialakulását vízzel molekulák).
Az ereje hidrogénkötések hozzájárul a dimerek, amelyek stabilak, még a gáz halmazállapotú.
Kémiai tulajdonságok savak
A szerkezet a karboxilcsoport
Karboxilcsoport egyesíti a két funkciós csoport - karbonil-csoport és hidroxilcsoport, kölcsönösen befolyásolják egymást:
A savas tulajdonságokkal karbonsavak fejezzük fényesen elég. Ez annak köszönhető, hogy a kölcsönös befolyás az atomok a karboxilcsoport. Az elektronsűrűség, amely kiszorítja a több elektronegatív oxigén hidroxilcsoport, amely gyengíti a kötést OH és megkönnyíti a szétválasztása hidrogénatom ,. E.oblegchaet disszociációs savat (ez azért van, mert a + M hatás érvényesül OH-csoport, mielőtt -I-hatás) . A mobilitási protonok található # 945-helyzetben is függ a szerkezet a COOH csoportok (a részletes magyarázatokat meghatározott előadásában „A aldehidek és ketonok”).
1) Savas tulajdonságokkal
Disszociációja savak. A vizes karbonsavat disszociál ionokra, és van egy savas reakció. Ez lehet kimutatni a mutató, amely tekinthető egy minőségi meghatározása savak. Például lakmusz pirosra vált.
A vizes oldat, a disszociációs folytatja a kialakulását stabilizált mezomer anion töltés delokalizáció.
határ rezonáns kommunikációs struktúra C-O igazítva
A mezo - jelenség összehangolása az elektronsűrűség a két oxigénatomot tartalmaz.
Karbonsav erősebb sav, mint az alkoholok.
Hangyasav - a legerősebb, hiánya miatt az elektron hatását az alkil-csoportok. Szubsztituensek pozitív indukciós hatás (elektron - CH3, C2H5) alacsonyabb savasság szakadás hidrogén az oxigén a OH-csoport nehezebb.
A sóképzés. Savak sóképzésre alkalmas fémekkel, ezek oxidjai és hidroxidjai.
a) reagáltatva fémek:
2RCOOH + Mg ® (RCOO-) 2 Mg + H2
b) reakció fém-hidroxidok:
2RCOOH + NaOH ® RCOONa + H2O
2) reakciói az OH csoport
Észterek képzése (R'-COOR „) - .. Ez a reakció egy észterezési reakció közötti alkoholokkal képezett jelenlétében ásványi savak A reakció reverzibilis.
ecetsav, etil-alkohol, etil-éter-ecetsavat
Savak lineáris szerkezetű, mint például az R-CH 2-COOH helyett reagálnak, mint az elágazó szénláncú sav: R 2CH-COOH, R 3C-COOH. katalizátort az észterezési reakcióban, H + ionok játszanak:
A reakció az alábbi mechanizmus: oxigén egy karbonilcsoportot és egy proton elfogja I. Ez képezi egy karbokation karbokation tulajdonít alkohol molekula miatt a magányos pár a oxigénatom a komplex II. II komplex, amely képes reverzibilisen alkotó karbokation bomlás és a III. során képződött disszociációs-észter (katalizátor - egy proton szabadul).
Nagy érdeklődés ebben a reakcióban a problémát: sav vagy hidroxil-alkoholban hasítjuk efiroobrazovaniya reakciót. A „nyomjelző” (18O nehéz izotóp) azt mutatja, hogy a keletkező vizet hidrogén és hidroxil-sav-alkohol.
(Ha jelzett alkoholban oxigén ezután képződött vizet tartalmaz közönséges oxigén)
Reakciók teljes csere az OH-csoport.
Származékok előállítására karbonsavak.
1) savhalogenidek állíthatjuk elő az intézkedés a foszfor-pentaklorid (PCI 5), tionil-klorid (SOCI2).
2) halogénatom halogenid magas reaktivitás, azonban halogenideket használunk acilezőszerként. Az így kapott sav-anhidridek.
Így például ecetsavanhidriddel (R = CH3) alkalmazunk a szerves szintézisekben, mint egy erős dehidratáló szerrel.
3) amidképzés ammónia végzik.
-amid, ammónium-sót
4) ammonolízis savak jelenlétében alumínium-oxid képződését eredményezi a nitrilek.
A reakciókat érintő hidrogénatomok találhatók # 945 szénatom.
A hidrogénatomok szembesülnek 945 # heiyzetében korlátozása savak fokozott mobilitása miatt elektronoottyagivayuschego karboxil hatását (lásd szerkezet tárgya „aldehidek és ketonok.”).
Különleges tulajdonságok van hangyasav. mert tartalmaz egy aldehid-csoport. Ezért ez a sav tulajdonságainak egy redukálószer, például ad egy ezüst tükör reakciót. A nitril hangyasav - nem több, mint egy tsinovodorodnaya H-CºN vagy hidrogén-cianid.
Használata egyes képviselőivel. Hatását az emberi egészségre
Hangyasavat alkalmazunk a gyógyszerek előállítására, növényvédő szerek, tartósítószerek, az textilfestékként, van egy baktericid hatását. Bőrrel való érintkezés égési sérüléseket okoz.
Ecetsavat használunk a termelés sói és észterei (acetátok), gyógyszerek, festékek és inszekticidek. Ez egy tartósítószer. Ez égési sérülést okoz.
Propionsav elengedhetetlen a szintézis a herbicidek polimerek.
Az alsó tagjai számos sav irritálhatja és légzési elégtelenséget. Monokarbonsavak mint oxidált intermedierei anyagcsere a szervezetben. Aromás savak (benzoesav) változatlan formában választódik ki.
Magasabb sav károsíthatja a májat és a vér összetételének megváltozását.
Zsírok - glicerin és magasabb vegyértékű karbonsavak.
Közönséges név az ilyen vegyületek - a trigliceridek vagy a triacil, ahol az acilcsoport - karbonsav maradékot -C (O) R.
A összetétele a természetes trigliceridek közé maradékok telített savak (palmitinsav C15H31COOH, sztearinsav C17H35COOH) és telítetlen (olajsav C17H33COOH, linolsav C17H29COOH).
A zsírok megtalálhatók minden növények és állatok. Állati zsírok (.. Mutton, sertés, marha, stb), jellemzően szilárd anyag, alacsony olvadáspontú (kivéve - halolaj). A zsírok főleg trigliceridekből limit savak.
A növényi zsírok - olajok (napraforgó, szójabab, gyapot és mások.) - folyékony (kivéve - kókuszolaj). A kompozíció a triglicerid olajok közé tartoznak maradéka telítetlen savak.
Folyékony zsírok alakítjuk szilárd egy hidrogénezési reakció (hidrogénezés). Amikor ez a hidrogént adagolunk az egész kettős kötést tartalmaz a szénhidrogéncsoport molekulák olajok.
Tehát kap olcsó „vaj” olaj. Ilyen olaj olcsó, de nem túl jó minőségű, akkor gyorsan lebomlik (avas).
A termék hidrogénezését olajok - szilárd zsír (mesterséges zsír, hidrogénezett zsír). Margarin - étkezési zsír keverékéből áll hidrogénezett olajok (napraforgó, kukorica, gyapot, stb), állati zsír, tej és ízesítőanyagok (só, cukor, vitaminok és mások.).
Zsírok észterek jellemzi reverzibilis hidrolízis reakció által katalizált ásványi savak. Részvételével lúgos hidrolízis zsírok zajlik visszafordíthatatlanul. A termék ebben az esetben a szappanok - sói magasabb karbonsavak és alkálifémek.
Nátriumsó - szilárd szappan, kálium - folyadék. Reakciója lúgos hidrolízis zsírok, és általában minden észterek is nevezik elszappanosítás.
Telítetlen savak: akrilsav és metakrilsav.
A legfontosabb képviselői a telítetlen savak:
akrilsav (propénsav) CH2 = CH-COOH
metakrilsav (2-metilpropenovaya sav)
Akrilsav tanítani szintetikusan. Ez egy folyadék, szúrós szagú. Könnyen polimerizálhatnak, így poliakrilsav.
Egy gyakorlati jelentősége az akrilsav-észterek, vagy inkább a polimerizációs termékek:
akrilsav-etil-észter
Poliakrilátok átlátható és használják a gyártás különböző műanyag és szerves üveg. Nagyobb keménységű összehasonlítva poliakrilátok rendelkeznek metakrilát - metakrilsav-észterek.
A legjobb szerves üveg plexi - polimetakrilsav-metil-észter. Plexiüveg használnak a gyógyászatban a gyártás protézisek.
metakrilsav-metil-észter
Általában, telítetlen savak jellemző számos reakció jellemző alkének: csatlakozás halogének, hidrogén a kettős kötés, oxidációt kálium-permanganát, a dién-szintézis.
Kétbázisú karbonsavak.
A legegyszerűbb kétbázisú sav - oxálsav (először találtak sóska) és etán-dikarbonsav. A következő reprezentatív - almasav vagy propándisav. Kétbázisú savak négy szénatomot vagy borostyánkősav nevezett butándisav.
A legfontosabb reakció az ilyen savak - előállítására kondenzációs polimerek.
olyan észterezési reakciókat, és az amidok előállítására a dikarbonsavak alapján az ipari termelés rendkívül fontos gyakorlati szempontból a kondenzációs polimerek.
A kondenzációs egy dikarbonsav és alkándiol képződéséhez vezet a poliészter. Poliésztereket széles körben alkalmazzák a szintetikus szálak előállítását.
Az egyik legfontosabb poliészter - poliészter - polikondenzációval előállított tereftálsav és etilénglikol.
A kondenzációs egy dikarbonsav és egy diamin képződéséhez vezet egy poliamid. Poliamidok előállításához használt szintetikus anyagok (szintetikus gyapjú). Egy fontos gyakorlati célokra Poliamid - Nylon 6,6 - polikondenzációval előállított adipinsav és hexametilén-diamin.
A kibővített formában a következőképpen néz ki:
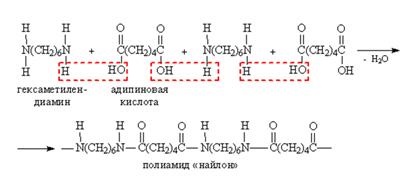
A „nejlon-6,6” neve az első szám jelzi a szénatomok száma a dikarbonsav és a második - a szénatomok száma a diamin.
Ha a keveréket vetjük alá a polikondenzációs folyamatot egy aromás dikarbonsavat (például, tereftálsav) és egy aromás diamin, a kapott poliamid anyagok összehasonlítható szilárdságú acélból készült termékek: