A mitokondriális légzési lánc és az oxidatív foszforiláció
Tárgy: a mitokondriális légzési lánc. oxidatív foszforiláció
1. Szerkezet a mitokondriális légzési lánc, a szekvenciája átadása protonok és elektronok. Formula hidrogén-akceptor,: NAD, FAD, KoQ. Szerepe az oxigén az elektron transzport lánc.
2. Az enzim komplexet a légzési lánc - a kompozíció, funkció. Transzmembrán potenciál, annak kialakítása és alkalmazása. A szerepe a belső mitokondrium-hártyán.
3. A koncepció az oxidatív foszforiláció. foszforiláció mértéke (meghatározás, méretezési példát). A szerepe az ATP szintáz. A fő irányok használata ATP a sejtben. ATP formula.
4. Energiamérleg (kitermelés ATP) aktív oxidációs-acetát (acetil-CoA) és piruvát.
5. A nem-foszforiíező vagy szabad szubsztrátok oxidációs - biológiai szerepe. Lekapcsolása oxidáció és foszforiláció a mitokondriumban.
6. Olyan anyagok, amelyek befolyásolják a folyamat oxidatív foszforiláció mitokondriumokban: légzés inhibitorok protonophores, ionofórok.
A légzési lánc és az oxidatív foszforiláció.
14.1.1. A reakciót a piruvát-dehidrogenáz, és a Krebs-ciklus történik dehidrogénező (oxidáció) szubsztrátok (piruvát, izocitrát, α-ketoglutarát, szukcinát, malát). Az eredmény Ezen reakciók termelnek NADH-t és FADH 2. Ezeket a csökkentett koenzimek oxidált forma a mitokondriális légzési lánc. Az NADH oxidációját és FADH 2 áramló conjugately ATP szintézis ADP és H 3PO 4 nevezik oxidatív foszforiláció.
Az áramkör felépítése mitokondriumok ábrán látható 14.1. A mitokondriumok intracelluláris organellum, amelynek két membrán: a külső (1) és a belső (2). A belső mitokondriális membrán formák számos redők - crista (3). Által határolt térben a belső mitokondriális membrán, az úgynevezett mátrix (4), által határolt tér a külső és a belső membránokat - intermembrán teret (5).
14.1 ábra. Az áramkör felépítése a mitokondriumok.
14.1.2. Légzési lánc - soros áramkör enzimek végzi A hidrogén-ionok és elektronok oxidációjával szubsztrátok molekuláris oxigén - a végső hidrogén-akceptor. E reakciók során az energia-felszabadulás fokozatosan, kis adagokban, és azt lehet tárolni ATP formájában. Lokalizálása légzési lánc enzimek - a belső mitokondrium-hártyán.
A légzési lánc négy multienzim komplex (ábra 14.2).
Ábra 14.2. Enzim komplexek a légzési lánc (jelzi parcellák konjugálásával oxidáció és foszforiláció):
I. NADH-KoQ-reduktáz (köztitermék tartalmaz hidrogént megkötő: flavin-mononukleotid és vas-kén fehérje). II. Szukcinát-KoQ-reduktáz (köztitermék tartalmaz hidrogént megkötő: FAD és vas-kén fehérje). III. KoQN 2 -tsitohrom c reduktáz (elektron befogadására, tartalmaz: a citokróm b és vas-kén fehérjék 1.). IV. A citokróm c oxidáz (elektron befogadására, tartalmaz: a citokróm-a és 3. rézionok Cu 2+).
14.1.3. A ubikinon (koenzim Q) járnak, mint közbenső hordozói elektronok és a citokróm c.
Ubikinon (KoQ) - zsírban oldódó vitamin-szerű anyag, amely képes arra, hogy könnyen diffundál a hidrofób fázisban a belső membrán a mitokondriumok. A biológiai szerepe a koenzim Q - elektron transzport a légzési lánc flavoproteinek (komplexek I. és II) a citokrómok (komplex III).
A citokróm c - komplex fehérje kromoprotein, amelynek prosztetikus csoport - hem - tartalmaz a változó vegyértékű vasat (Fe 3+ oxidált formában és a Fe 2+ a redukált forma). Citokróm c jelentése egy vízben oldható vegyületet található és a periférián a belső mitokondriális membránon keresztül a hidrofil fázisban. A biológiai szerepe a citokróm c - elektron transzport a légzési láncot a komplex III komplex IV.
14.1.4. A közbenső elektron-hordozó a légzési láncban vannak elrendezve aszerint, hogy azok redoxpotenciálok. Ebben a szekvenciában, a képesség, hogy adományozni elektronok (oxidálódik), csökken, és a képesség, hogy csatolja elektronok (vissza) növeli. Legnagyobb képességet adományozni elektronok van NADH legnagyobb képességet, hogy csatolja elektronok - molekuláris oxigént.
Ábra 14.3 ábra a tervezés bizonyos részét a reakcióképes köztitermék hordozói elektronok és a protonok a redukált és oxidált formája, és ezek egymásba való átalakítását.
Ábra 14.3. Interkonverzióját oxidált és redukált formájának közbenső hordozók elektronok és protonok.
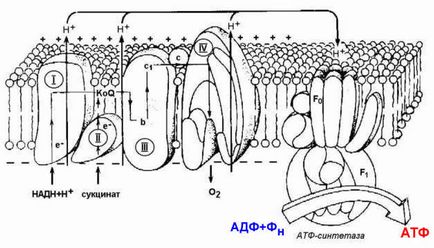
Ábra 14.4. Hely légzési lánc enzimek és az ATP-szintáz, a belső mitokondrium-hártyán.
A protonok intermembrán térben származó miatt elektrontranszfer energia, mozgassa ismét a mitokondriális mátrixban. Ezt a folyamatot úgy végezzük, hogy az enzim H + -függő ATP-szintetáz (H + -ATP-áz). Az enzim két részből áll (lásd a 10.4 ábra.): A vízben oldható része a katalizátor (F 1), és elmerül a hidrofil membrán csatornát (F 0). Átmenet a H + ionok egy régió nagyobb, hogy alacsonyabb koncentráció kíséri megjelenése szabad energia, ami miatt az ATP szintetizálódik.
14.1.6. A felhalmozott energia formájában ATP-t, használjuk a szervezetben különböző biokémiai és fiziológiai folyamatokat. Emlékszik az alapvető példák segítségével energiát ATP:
1) szintézise komplex vegyi anyagok egyszerűbb (anabolizmus reakció); 2) izom-összehúzódások (mechanikai munka); 3) képződése transzmembrán biopotentials; 4) az aktív anyagok szállítására át a biológiai membránokon.
14.2.1.Stepen konjugálása oxidáció és foszforiláció mitokondriumokban jellemzi foszforiláció aránya (F / G). Ez az arány a szervetlen foszfát mennyiségét molekulák (H 3 O 4 P) vezetjük át ATP elfogyasztott mennyiségének oxigénatomok (O 2).
Például, ha a hidrogéndonor a légzési lánc a molekula NADH. az elektronok a donor (NADH), hogy egy akceptor (oxigén) 3 oldalak konjugáció oxidációs és foszforiláció (I, III és IV enzim komplexeket a légzési lánc). Így, ezt ki lehet alakítani maximálisan 3 ATP molekulák (ADP 3 + 3 H 3PO 4 → 3 ATP). 1 fordított oxigén (O 2 H + → H 2 O). A koefficiens F / G = 3/1 = 3.
Ha a hidrogéndonor a molekula FADH 2 a légzőkörben rész 2 elektront átadni konjugációja oxidáció és foszforiláció (III és IV enzim komplexeket a légzési lánc). Így, ezt ki lehet alakítani maximálisan 2 molekula ATP (2 ADP + 2 H 3PO 4 → 2 ATP). Fogyasztják, ahogy az előző esetben, 1 oxigén (O 2 H + → H 2 O). A koefficiens F / G = 2/1 = 2.
14.2.2. Egy összetettebb példáját az együttható számítás foszforiláció - az oxidációs piruvát végtermékek - ábrán látható 14.5. Ez az útvonal történik dehidrogénező 4 szubsztrátok (piruvát, izocitrát, α-ketoglutarát és malát) alkotnak NADH-t és egy hordozót (szukcinát) FADH 2 képezve csökkentett koenzim oxidált a légzési lánc, és a foszforilációs reakcióban előállított konjugátum (4 × 3 ATP + ATP 1 × 2) = 14 ATP molekulák. Több 1 molekula ATP (GTP) van kialakítva szubsztrát foszforiláció a szukcinil-CoA. Így a teljes oxidációja 1 molekula piruvát alakult 15 molekula ATP (14 közülük - oxidatív foszforiláció).
Összegének kiszámításához felhasznált oxigén, meg kell tudni, hogy a több dehidrogénezés helyén a metabolikus utat. Minden egyes oxidációja redukált formáját a koenzim szükséges 1 oxigénatom (cm. Fent). Ezért, a mi példánkban azt elfogyasztják 5 oxigénatomot. Az érték a P / O arány értéke 14/5 = 2,8.
Ábra 14.5. A számítás az energiamérleg oxidatív dekarboxilezése piruvát és Krebs-ciklus.
Lekapcsolása légzés és a foszforiláció.
14.3.1. Az átadás az elektronok a légzési lánc nem minden esetben fordul elő Kapcsolódik a foszforilációja ADP. A állapot, amelyben szubsztrátok oxidáció a légzési lánc fordul elő, de az ATP nem képződik, az úgynevezett szabad (nem-foszforiíező) oxidáció. Az energia oxidációja során felszabaduló eloszlik a hő.
Lekapcsolása oxidáció és foszforiláció a mitokondriumban is előfordulhat bizonyos patológiás körülmények között. A fő tünetek az ilyen állapotok lehetnek a fáradtság, láz, fogyás ellenére fokozott étvágy, légszomj és szívdobogás.
14.3.2. Disszociációja oxidáció és foszforilezés hatása által okozott számos anyagok, mind a természetes és szintetikus. A hatásmechanizmusa ezen anyagok abban áll, hogy azok hordozói protonok a membránon keresztül. Anyagok disszociatív oxidáció és foszforiláció, osztható protonophores és ionofórok.
Protonophores olyan gyenge szerves hidrofób savak, amelyek anion formájában (R-COO -) kötődnek protonok intermembrán térben, diffúz át a membránon, és disszociál egy mátrixban alkotnak protonok. Ebbe a csoportba tartoznak, például, szabad zsírsav, a pajzsmirigy hormonok, szalicilátok, dikumarol, 2,4-dinitro-fenol (lásd. Ábra 14.6).
Ábra 14.6. A hatásmechanizmus 2,4-dinitro-fenol.
Ionofórok (valinomycin, nigericint, gramicidin) képesek kell építeni a membránt, egy olyan csatornát képez, amelyen keresztül tud mozogni a protonok és más egyértékű kationok - Na + vagy K + (ábra 14.7). Ennek eredményeként, a lehetséges proton eltávolítjuk és az ATP szintézis megbomlik.
Ábra 14.7. Valinomycin megkönnyíti celluláris felvételének H + ionok.