Tanulmány az emissziós spektrum atomos hidrogén a látható tartományban (Balmer sorozat)
Név: Ahhoz, hogy tanulmányozza az emissziós spektruma atomos hidrogén a látható tartományban (Balmer sorozat)
Tárgykörben: fizika
Leírás: Lab № 16 VIZSGÁLAT emissziós spektruma atomos hidrogén a látható Balmer sorozat Célkitűzés: Annak meghatározására, gyakoriságának spektrális vonalak a látható spektrumban, és emissziós hidrogén értékének kiszámításához a Rydberg állandó. berendezés:
Fájl mérete: 69.5 KB
Job letöltve: 18 fő.
Lab № 16
VIZSGÁLAT emissziós spektruma atomos hidrogén a látható tartományban (Balmer sorozat)
A cél a munkát. meghatározzák a frekvenciák spektrális vonalak a látható spektrumban, és emissziós hidrogén értékének kiszámításához a Rydberg állandó.
Felszerelés. hidrogén-lámpa, neon lámpa, a lencse, a monokromátorral 2 vagy PA-MUM.
Rövid elméleti információk
Fénykibocsátás történik részletekben atomok # 150; sugarak az átmenetet az elektron egy atom az egyik állandósult állapotban egy másik, több energiát alacsony. A fotonenergia egyenlő h . ahol h # 150; Planck-állandó,
# 150; frekvenciája a kibocsátott sugárzás.
Szerint kvantummechanika, frekvencia függ az energia a stacionárius állapot az elektronok az atom az alábbiak szerint:
ahol E n és E k # 150; A kezdeti és a végső energia a stacionárius állapot az atom, illetőleg; k # 150; száma az energia szintjét az atom, amely készült elektron átmenet után sugárzás, N # 150; szint száma, amelyből egy elektron mozog, amikor az atom emissziós elektromágneses energia. R # 150; Rydberg állandó; c = 3 ∙ augusztus 10 m / s # 150; fény sebessége vákuumban.
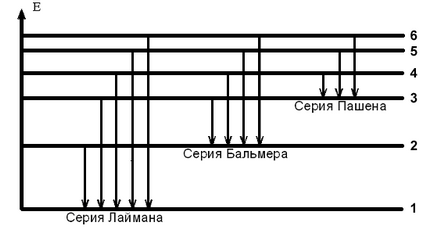
hidrogén spektrális vonalak vannak csoportosítva sorba (lásd. 1. ábra).
Lyman sorozat vonalak történik az átmenet az elektronok a magasabb energia stacionárius állapot az első. Mert ezeket a sorokat
k = 1, n = 2, 3, .... és a frekvenciák a láthatatlan ultraibolya tartományában a spektrum.
A vonalak a látható része a spektrum # 150; Balmer sorozat # 150; azzal jellemezve, elektron átmenetek a államok a számok n = 3, 4, 5, ... az állami
a k = 2 Az átmenet az elektron állapotban n = 3 állapotba k = 2 megfelel a piros vonal a spektrumban, az átmenetet a állapotban n = 4 állapotban a k = 2 # 150; zöld-kék vonal, és egy átmenetet egy állami n = 5 állapotban a k = 2 # 150; lila vonal a hidrogén-spektrum.
Transitions elektronok szintben száma k = 3 a magasabb energia szintje formájában egy sor olyan Paschen vonalak, amelynek frekvenciák vannak a láthatatlan infravörös tartományban és a t. D. Minden spektrális vonal megfelel egy bizonyos gyakorisággal és hossza hullám. rokonságban
Ebben a cikkben, azt kell kísérletileg meghatározni a frekvenciákat a három vizsgált vonalak a Balmer sorozat. A kapott eredményeket, a következő képlettel számítjuk (1) Rydberg állandó.
Frequencies hidrogén-spektrumot egy monokromátorral UM-2, optikai rendszer ábrán látható. 2. A fény hidrogénatom lámpa 1 által van fókuszálva lencse 2 ra a belépő rés monokromátor 3. A rés van a hangsúly a 4 lencse, és belép a mozgatható részt a monokromátor, az úgynevezett kollimátor. Forgassa a gombot 5 lehet mozgatni az optikai tengely mentén a kollimátor. Coming lencsét 4 párhuzamos fénynyalábot esemény a 6 prizma és egy spektrumot. Lens 7 koncentrál a spektrumot a területen a megfigyelés. Nyomon követése spektrum szemlencsén keresztül 8. A szemlencse egy recézett gyűrűt, amely lehet elérni elforgatásával a legélesebb minta megfigyelés spektrum. Alján a rés 3 mikrométercsavarral, amely lehetővé teszi, hogy módosítsa a rés szélessége.
képet a spektrum megfigyelt bevezetésével a közepén a látómező a jogot a területen. Erre a dobot 9 elfordul jobbra a távcső monokromátor. A dobot, amely egy skálával, amely lehetővé teszi, hogy meghatározzuk a forgatást fokokban. A skála időköz 2 . Gróf spektrális vonalak termelt idején kombinálásával összhangban nyíl # 150; pointer közepén a látótér. Arrowhead és egy kép a spektrum figyelni kell egyformán élesen. Ehhez állítsa be a szemlencse éles nyíl-mutató órát, majd forgassa el a gombot az 5. elérni éles képet a spektrum ellenőrzés. A belépő rés van egy szelep 10, megszakítva a fényáram. A dolgozó helyzetben a csappantyú kell nyitni.
A skála dob sorolt frekvenciákon. Erre a célra, egy jól tanulmányozott neon emissziós spektruma, táblázatban leírt. 1.
Leírás neon emissziós spektrum
Megjegyzés. Ahhoz, hogy megkönnyítse a megfigyelés a piros vonal 1. A piros # 150; narancssárga vonal a 2. és 3. sor minden sárga, piros és sárga része a spektrum neon látható egy külön ábrán a laboratóriumi asztalra.
Az, hogy a teljesítmény
1. Telepítse az optikai vasúti neoncső sugárzás és irányítsa rá a belépő rés monokromátor. Állítsa be a minimális rés szélessége. Megfigyelése révén a szemlencse spektrumát neon, egyesítik a nyíl mutató egyes vonalak táblázatban ismertetett. 1. Az elfordulási szög a dob skála és a hullámhossz a táblázat. 1 minden sorban adja meg
Táblázat. 2. Mozgó a fényes vörös, narancs és sárga vonalak gyenge vonal, a zöld és a kék régiók a spektrum, szükség van, hogy fokozatosan növelje a rés szélessége.
Száma neon színképvonal
2. A adattábla. 2, hogy egy kalibrációs görbe a forgási szög a frekvencia. Ha grafikusan ábrázoljuk tartsák be a következő skála szerint. A tengely „frekvencia” 1 cm kell felelnie ∙ 10 10 12 Hz, a tengelyen „szög forgási” 1 cm kell felelnie 100 dob forgása.
4. Add a jegyzetfüzetbe táblázat. 3 leolvasás a skála dob megfelelő minden egyes megfigyelt spektrális vonalak hidrogén.
5. A felépített kalibrációs görbe meghatározásához frekvenciaspektrum vonalak hidrogén.
6. ábra. 1 készlet számok n és k szintjét a kezdeti és a végső elektron állapot minden sorban spektrumát hidrogénatom. Az eredményeket a táblázatban. 3.
7. Az (1) képletű kiszámításához Rydberg esetében, mindegyiknél állandó Balmer vonalak. Az átlag értékét a Rydberg állandó, és összehasonlítjuk a táblázatos értéke R = 1,097 ∙ július 10 m -1.
A spektrális vonal hidrogén
Forgásiszögét (fok)
Száma felső szinten n
Száma az alsó szinten
Rydberg
R (m-1)
1. Miért a kalibráló sor neon? Tudom használni egy sor más elemeinek a sugárzás?
2. lista a sorozat a hidrogén-spektrum. Melyik átmenet felel meg a fejét minden sor a sorozat?
3. Mi határozza meg a határ a sorozat? Miért van a határ sorozat intenzitása csökken?
4. Hogyan átmenetek megfelelnek vonalak a látható része a spektrum hidrogén? Mi a spektrális sorozat?
a laborba száma 16
Csakúgy, mint más feladatok érdeklődésére esetleg számot
Maroussia Churai Kostenko Lіna ROZDІL I Yakbi znayshlas Égő könyv Pid óra Pozhezhi Poltavі 1658 roku zgorіli OAO Minden dokumentumot mіskih hajók ref. A mozhlivo Szered közülük b tudni jobb Marusі Churai. Jobb tsya rozglyadalasya egyik sudіv s meghajtó vbivstva Kozak.