Molekuláris kinetikus elméletét az első, második, harmadik pozíció
Az első pozíció a molekuláris kinetikai elmélet
Az anyag részecskékből áll.
Molekula - a legkisebb részecske egy anyag, amelynek alapvető kémiai tulajdonságai.
A molekula atomokból áll. Atom - a legkisebb részecskék az anyag, amely nem osztható a kémiai reakciókban.
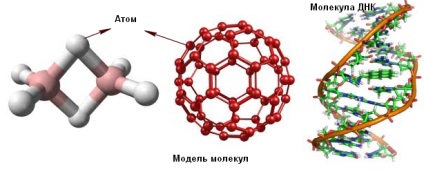
Sok molekulák két vagy több atomot tartanak össze kémiai kötéseket. Egyes molekulák állnak több százezer atom.
A második pozíció a molekuláris-kinetikai elmélet
A molekulák állandó véletlenszerű mozgásban. Ez a mozgás nem függ a külső körülményektől. Mozgás előre nem látható módon miatt molekuláris ütközések. Bizonyíték van Brown-mozgás a részecskék (nyitott R.Brounom 1827). A részecskéket helyezzük egy folyékony vagy gáz, és figyeljük a kiszámíthatatlan forgalom miatt ütközések molekulákkal az anyag.
Bizonyíték kaotikus mozgás diffúziós - penetráció molekulák az anyag közötti hézagok a másik anyag molekulái. Például, az illata légfrissítő, úgy érezzük, nem csak azon a helyen, ahol azt permetezzük, de fokozatosan összekeverjük a levegő molekulák a szobában.
Halmazállapot
A gázok, az átlagos távolság molekulák között is százszor nagyobb, mint a méret. Alapvetően molekulák mozognak fokozatosan és egyenletesen. Követve az összecsapások forogni kezd.
Folyadékokban, a távolság a molekulák sokkal kevésbé. Molekulák rezgési végre, és haladó mozgása. Molekulák révén kis időközönként hirtelen átmenetet az új egyensúlyi helyzet (megfigyelhetjük folyadékáramlás).
A szilárd molekulák ingadozhatnak nagyon ritkán mozgott (csak akkor, ha a hőmérséklet növekszik).
A harmadik helyzetében a molekuláris-kinetikai elmélet
A molekulák között létezik interakció erők, amelyek az elektromágneses jellegűek. Ezek az erők segítenek megmagyarázni előfordulása rugalmas erők. Amikor az anyag összenyomódik, a molekulák közelebb egymáshoz, az erő a taszítás közöttük, amikor a külső erő elhalasztja molekulák egymástól (feszített anyagból) vonzóerő lép fel közöttük.
az anyagsűrűség
Ez skaláris érték, ami által meghatározott képlet
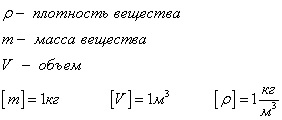
Density anyagok - lásd a táblázatot értékek
A kémiai jellemzőit az anyag
Avogadro számát NA - atomok száma szereplő szénizotóp 12g
Az anyagmennyiség - aránya az elemek száma az anyag a Avogadro-szám

1 mól bármely anyag tartalmazza ugyanazt a részecskék száma, ez a szám egyenlő a Avogadro-állandó.
A moláris tömeg M - a tömege egy mól anyagra
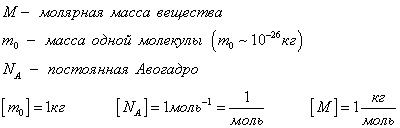
Ha a test tartalmaz N molekulatömeg m0. a súly
A részecskék koncentrációja - a részecskék száma a mennyiség
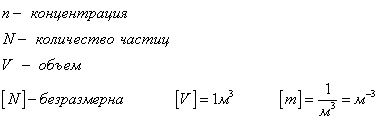
Akkor abból a képlet