Állami beleesik a megoldás - studopediya
Alapfogalmak és osztályozása kolloid felületaktív
Kolloid felületaktív azzal jellemezve, alacsony valódi oldhatóság és a képességét, hogy csökkentik a felületi feszültséget és a határfelületi feszültséget. Azonban, ezzel együtt egy bizonyos koncentráció, az úgynevezett kritikus micella koncentrációja (CMC) az oldat kezd aggregátumokat képeznek a molekulák - micellák, miáltal a teljes oldhatóság a felületaktív növekszik hirtelen, mivel a molekuláris oldhatóság állandó marad, és egyenlő a CMC.
A felületaktív anyag képes volt micellákat képezni, meg kell felelniük két követelménynek:
van egy elég nagy szénhidrogén-csoport, amely csökkenti oldhatósága vízben;
elég erős poláros csoport hozzájárul annak oldhatóságától.
Ezeket az igényeket elégíti, nem minden felületaktív anyagot, például, a homológ sor alifás alkoholok micella képződést nem jellemző. A vegyületek szénatomszáma kevesebb, mint 7 micella megakadályozza rövid szakaszon a szénhidrogéncsoportok, és a magasabb homológok - viszonylag alacsony gidrofilnoyst poláris csoport.
Kolloid felületaktív szerinti szerkezeti jellemzői a molekulák vannak osztva három fő csoport: anionos, kationos, nemionos.
Az anionos felületaktív anyag disszociál vízben alkotnak egy negatív töltésű felületaktív ion. A adszorpciója felületaktív anyag az oldatból adszorbeálódik a felületén az anionok és a felület szerez egy negatív töltés. A legfontosabb képviselői ennek a csoportnak a felületaktív anyagok a kolloid hagyományos szappanok és szulfonsavak sói a molekuláris lánc, amely a szénatomok száma nem kevesebb, mint 10, és nem több, mint 22. Amikor a nagyobb hossza szénhidrogén lánc szappanok vízben oldhatatlanok. Technikai célokra különösen fontosak nátrium-szappanok a palmitinsav, sztearinsav és olajsav, telítetlen. Ez - a nátrium-palmitát C15 H31 COONa, nátrium-sztearát C17 H35 COONa-oleát és nátrium-C17 H33 COONa. Példa disszociációs nátrium-oleát:
Szappanok a kettő- és háromértékű kationokkal (kalcium, magnézium, alumínium, stb) vízben oldhatatlanok, de képeznek kolloid rendszer szénhidrogén médiában. Ezeket kenőzsírokhoz ásványi olajban, és az emulziók stabilizálására, (w / o).
A tisztító hatású nemcsak zsírsavak, hanem sói nafténsavak termelt a tisztítási a kerozin és dízelolaj.
A kolloid felületaktív, amely aktív szulfocsoport sók közé tartoznak a nagy molekulatömegű szulfon általános szerkezetét CnH2n + 1, C6 H4 SO3 M - alkil-aril-csoport (amelyben m - Na + K + NH4 + ..). Ez magában foglalja a sók, alkil-helyettesített naftalinszulfonsavak, például nátrium-butilnaftalinsulfokisloty izo (Nek).
Széles körben használják a felületaktív anyagok és alkil - ethersulfates magasabb alkoholok és ezek sói (C17 nH 2n + 1 - O - SO3 M).
A kationos felületaktív anyag disszociál vízben alkotnak egy pozitív töltésű felületaktív ionok. Oldataiból ilyen felületaktív anyagok adszorbeált kationok felületén, ami így gátat pozitív töltésű. A kationos felületaktív anyagok, mérgező és általánosan használják mikrobicidek, és fertőtlenítők.
A kationos felületaktív anyagok oktadetsilammoniyhlorid (C18 H37 NH3 Cl); sói kvaterner ammónium bázisokkal, például, cetiltrimetilammóniumkloridot [C16 H33 (CH3) 3 NCI]; piridin-vegyületek szubsztituált a nitrogénatomon, például cetil-piridinium-klorid. Mindezen anyagok a vízben bonthatók anionok Cl -:
A nemionos felületaktív anyagok (nemionos felületaktív anyag). A molekulák nemionos felületaktív anyagok nem képesek a disszociáció. Az amfolitikus felületaktív anyagok, mint molekula, amely egy hosszú szénláncú szénhidrogén polárosabb, de a nem-ionos csoportokat végén, okozza a oldhatósága ezen anyagok. Ilyen csoportok hidroxil- vagy éterben. Ilyen felületaktív anyagok például az olyan vegyületek, előállíthatók olyan poliol molekulák több molekula etilén-oxid:
Oxi-etilén-láncnak van egy hidrofilitást való kölcsönhatás miatt a éteres oxigénatomon vízmolekulák, és adduktumok szert vízben való oldhatóság. Az előnye, oxietilén felületaktív az a képesség, a saját szintézisét hidrofilitásának beállítására nemcsak megváltoztatásával szénatomok száma a hidrofób láncban hanem a több oxietilén csoport. Kapott anyagot előre tulajdonságait. Egy másik jellemzője ezeknek anyagok, hogy azok nem képeznek sókat, és ezért könnyen oldható kemény vízben.
Jelenleg már sok száz kolloid szintetikus felületaktív anyagok. Egy fontos jellemzője a molekulák, ami elengedhetetlen a felületi és térfogati tulajdonságokkal, és így azok alkalmazását az aránya a két ellentétes csoportok molekulák - hidrofil és hidrofób (lipofil), egy úgynevezett hidrofil-lipofil egyensúly (HLB). Jelenleg nincs szigorú elmélet kiszámításához HLB. Ennek első közelítés használja a szemiempirikus rendszert, amely lehetővé teszi, hogy számszerűsíteni, és kifejezett kondicionált csoport számok fokú vízzel való kölcsönhatás, külön csoportokban, amely felületaktív anyagot molekulát. Csoport hidrofil csoportok a pozitív és lipofil - negatív.
HLB-száma különböző felületaktív lehet számítani szerint a speciális képletek mint a mennyisége a csoport szám, vagy kísérleti úton határozzuk meg. Minél több a mérleg van tolva, hogy a hidrofilitás, a nagyobb a szám a HLB. A száma nemionos felületaktív anyagok a HLB értéke kisebb, mint 20, az ionos felületaktív anyagok, mint például a kálium-oleát, ez egyenlő 20, és a kálium-lauril-szulfát - 40. HLB-számokat határozzuk régió felületaktív alkalmazások. Az emulziók / m HLB értékek változnak 3-6; nedvesítésére - 7-9; tisztítószerek számára - 13 és 15, és emulziós típusú O / W, jellegétől függően az olaj 8 és 18. A HLB rendszer formális, hogy körének meghatározása a felületaktív anyag nélkül jellemző a hatékonyság.
Igaz felületaktív megoldásokat. A lehető legmagasabb koncentráció, amelynél még kolloid felületaktív a vizes oldatban a molekuláris (ionos) formában, azaz. E. A kritikus micella koncentrációja (CMC) kicsi, és között változik 10 -5 -10 -3 mol / l. Szappanok, amelyek gyenge elektrolitok oldatban és ionok formájában (RCOO- -. M +), és abban a formában a molekulák (RCOOM), és mivel a termékek azok hidrolízise - zsírsav-molekulák (RCOOH). A erős savak sói, mint például szulfonsavak oldatban ionok formájában, és a nemionos felületaktív anyagok - formájában disszociálatlan molekulák.
Okok micella. Fent a CMC a vizes oldatok, és elkezdi az aggregáló molekulák micellák. Államban micellaképzése lehet tekinteni, mint egy megfordítható egyensúlyi engedelmeskedik a tömeghatás törvénye. Ez az egyensúly molekulák nemionos felületaktív leírható az egyenlet mX Û (X) m.
Egy másik megközelítés a ez a jelenség azon a feltételezésen alapul, hogy a micellaképződést egy új szakasz a kialakulását a vízrendszer - felületaktív anyagot. Így micellák tekintik egyfajta fázis maximális diszpergálhatóságot (pseudophase), mert ellentétben igaz fázisszétválás micella képződést nem vezet egy végtelenül nagyszámú molekula az egység (a molekulák számának az egység nevezett aggregációs szám). Támogatása ez az elmélet, hogy egyrészt, a koncentráció az oldott felületaktív állandóság felett CMC; Másodszor, a jelenlétében CMC éles törje meg a görbék a fizikai-mechanikai tulajdonságok - koncentráció.
Az összesített felületaktív molekulák van kialakítva szénhidrogénláncok, és hidrofil részei a molekulák találhatók a külső felületén a micella. A fő oka a aggregátumok vizes oldatai szénhidrogénláncok intermolekuláris erő, amely nagyobb, mint a kölcsönös vonzás a vízmolekulák és hidrokarbon láncok. Víz molekulák, mint a „push” a megoldás a szénhidrogénláncok, amely csökkenése kíséri az entalpia a rendszer. Micellákat képezni gátolják kölcsönös taszítása a hidrofil rész felületaktív anyag molekulák. Az ionos felületaktív anyagok ennek taszítás miatt elektrosztatikus kölcsönhatás hasonló töltésű ionos csoportokat, a nemionos felületaktív anyag - ozmotikus erők, hogy merülnek fel, mert a magasabb koncentrációjú a oxietilén láncok a perifériás része a micellák.
A szerkezet a micellák. Alacsony koncentrációjú vizes oldatok kolloid szemcseméret és a felületaktív anyag molekuláris oldott molekulák az oldatban szabadon mozog, egymástól függetlenül. Amikor a koncentrációja PFC kezdődik alkotnak úgynevezett micellák Hartley. képviselő gömb alakú aggregátumok, amelyekben a szénhidrogén láncokat a molekulák összefonódik egymással, és a poláris csoportok a külső (a víz). A számos felületaktív molekulák egy ilyen aggregátum 50-100, de elérheti akár a 1000. A átmérője ilyen gömb alakú aggregátum mintegy kétszerese a hossza a felületaktív molekulák, amelyből képződik.
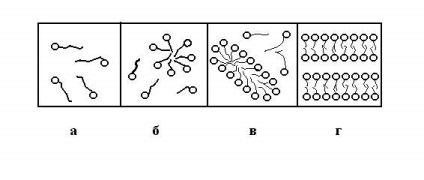
Ábra. 12.1. Reakcióvázlat kolloid micellaképződést felületaktív anyag:
és - a molekuláris híg felületaktív anyag oldat; b - felületaktív anyag oldatával gömb alakú micellák; egy - felületaktív anyag oldatot lemezes micellák; g - a koncentrált micelláris oldatot a felületaktív anyag
A szerkezet gömb alakú aggregátumai ionos felületaktív anyagok nagyon hasonlóak a hagyományos kolloid micellák. Az aggregálódott szénhidrogénlánc, alkotnak egyfajta csepp folyékony szénhidrogén szerepet játszanak a micella aggregált, részben disszociált ionos csoportokat jelen a vízben, így egy elektromos kettős réteg felületén a micellák (ábra. 12.2).
Amikor a koncentrációja az oldat növeli micelláris mérete és megváltoztatja formájukat. A szénhidrogén-láncok vannak elrendezve egymással párhuzamosan, és formájában micellák kezdődik rudak (ris.12.1, c), majd a lemezeket álló két sor felületaktív molekulák orientált egymással szénhidrogénláncokat (ris.12.1g). Egy további növekedése koncentráció vezet vegyületet micellák egymással és gélképződés mutatja a mikroszkóp alatt egy szabad álló struktúra, mint a szalagok és fóliák.
A létezése lemezes micellák meglehetősen koncentrált oldatok javasolt először Mac Ben, így gyakran hívják micellák Mak Ben
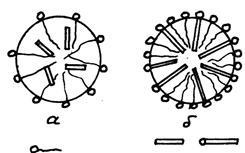
Ábra. 12.3. Reakcióvázlat szolubilizáló szénhidrogén (a), és a poláros
szerves anyagok (b) a felületaktív anyag micellák
Meghatározása CMC azon a tényen alapul, hogy a képződése során a micellák megváltoztatja a tulajdonságait a felületaktív anyag oldata. Nefeiometriás módszerrel találtuk, hogy az a micellák vezet hirtelen megnő a fényszórás felületaktív megoldást annak a ténynek köszönhető, hogy ez válik a heterogén.
A CMC felületaktív oldatok befolyásolhatja számos tényező. Így a CMC csökken a molekulatömeg növekedésével szénhidrogén lánc felületaktív. Egy ilyen függőség világos, mert egy igazi oldhatósága lánchossz növekedésével növekszik és csökken az a tendencia, felületaktív molekulák a társulásra.
Hőmérséklet hatása a CMC eltérő ionos és nemionos felületaktív anyagok. Az ionos felületaktív anyagok CMC általában növekszik a hőmérséklet emelkedésével miatt megsemmisítése aggregátumok miatt termikus mozgás a molekulák. De ez a hatás kicsi, mivel gyengíti a hidrofób kölcsönhatások, így a hőmérséklet hatását a CMC a gyengébb, annál kifejezettebb hidrofób felületaktív tulajdonságai. A nemionos felületaktív anyag CMC mindig növekvő hőmérséklettel csökken, mivel a hidrogén-kötések közötti oxigénatom az éter és a vízmolekulák elpusztulnak, oxi-etilén láncok dehidratálására és csökkenti azok kölcsönös taszítása, megakadályozza az aggregálódást.
Szolubilizációs A felületaktív oldatokban. A szolubilizálás fontos tulajdonsága felületaktív oldatok, amelyek miatt micellás szerkezetét. Beadva egy elegendően koncentrált felületaktív oldatokban gyakorlatilag oldhatatlanok vízben, szerves anyagok (alifás és aromás szénhidrogének, olajban oldódó festékek) tarthat kolloidálisan oldott. vagy oldódik. Ennek eredményeként a termodinamikai egyensúlyi formája átlátható megoldásokat. Egy anyag, amely oldódik a felületaktív oldatok nevezzük szoiubiiizátum.
Szolubilizáló képessége felületaktív változik mennyiségű kolloidálisan oldott szerves anyag a felületaktív homológ sorozat hosszúság növekedésével egyre nagyobb a szénhidrogén-csoport.
Száma szolubilizált anyagot arányosan nő a koncentráció a felületaktív anyag oldata az létezési tartománya gömb alakú micellák és meredeken emelkedik kialakulása alatt lamelláris micellák.
szénhidrogén szolubilizálása is növeli a növekedés a molekulatömegével, beadva szolubilizátumban poláris csoportokat.
A szolubilizálás oldódó szerves anyagok a felületaktív anyag micellák. Poláros szénhidrogének feloldjuk a mag micellák (12.3 ábra, a.), És a poláros szerves anyagok (alkoholok, aminok) található, a micellák úgy, hogy a szénhidrogén láncok befelé micella és a poláris csoportok - a vizes fázisban (12.3 ábra, b). .
Amikor szolubilizáló felületaktív anyag micelláris tömege növekszik nemcsak felvétele miatt a molekulák szoiubiiizátum, hanem azért is, mert a növekvő száma felületaktív molekulák micella. Fokozott hidrofobicitás micella mag, így az egyensúly fenntartása kell számának növelése a felületaktív molekulák alkotó micella.
Amikor egy lamelláris micellák szolubilizálására szerves anyag jut a micellák, ülepítő végei között a szénhidrogén molekulák és molekuláris láncok elválás rétegek (ábra. 12.4).
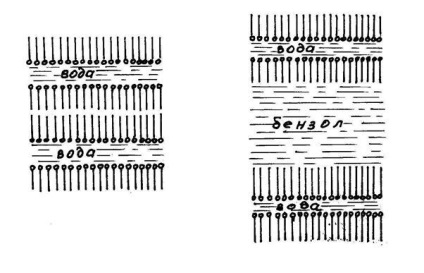
Ábra. 12.4. Szolubilizálása benzol lamelláris micellák:
és - micelláris oldatot előtt oldhatóvá; b - az azonos feloldás után.
A gyakorlati jelentősége kolloid oldatok felületaktív anyagok. Kolloid felületaktív anyagok nagy gyakorlati jelentősége van. Értékes műszaki felületaktív tulajdonságok miatt sem micellákká oldatban vagy nagy a felületi aktivitása, azaz. E. Képességük alkotnak molekuláris felületi adszorpciós réteg, amelynek stabilizáló hatását.
A legfontosabb tulajdonsága kolloid oldatok felületaktív - ez detergens.
Szolubilizációs egyik legfontosabb tulajdonságai micelláris oldatok, amelyek meghatározzák széleskörű alkalmazásra promyschlennosti és otthon. Ez az emulzió polimerizálás, az élelmiszer termékek, gyógyszerek előállítására és mások.
Az utóbbi években egyre fontosabbá válik micelláris katalízis, t. E. végezve a szintézist oldatban felületaktív anyagok a fenti a CMC. Megfelelő választás a felületaktív anyag nyújthat növekedését a reakció sebessége közötti ötezer alkalommal.
Az egyik legfontosabb alkalmazása micelláris rendszerek - alkalmazásuk fokozott olajkitermelés kutak.
Összefoglalva, hangsúlyozni kell, hogy a kettős jellege a felületaktív anyag (amfifil, és ennek következtében a létezését molekulák és micellák) az alapja az egyediségét a tulajdonságokat, amely meghatározza a jelentős és néha döntő szerepet sok ilyen anyag tekinthető kolloid-kémiai jelenségeket.